
下列有關一定物質的量濃度的溶液配制的過程中,造成所得的溶液濃度偏大的是
| A.要配制100 mL 1 mol·L-1 NaOH溶液,需在白紙上稱4 g NaOH固體,并且稱量速度較慢 |
| B.稱量時托盤天平的砝碼已被銹蝕 |
| C.溶解或稀釋溶質時燒杯尚未干燥 |
| D.定容時蓋上瓶蓋,搖勻后發現液面低于刻度線,再繼續滴加蒸餾水使液面重新達到刻度線 |
 快樂5加2金卷系列答案
快樂5加2金卷系列答案科目:高中化學 來源: 題型:單選題
設NA為阿伏加德羅常數的值,下列敘述正確的是:( )
| A.常溫常壓下,22.4 L乙烯中C—H鍵數為4 NA |
| B.1 mol羥基中電子數為10NA |
| C.在反應KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2轉移的電子數為6 NA |
| D.常溫下,1 L 0.1 mol/L NH4NO3溶液中NH4+的數目小于6.02×1022 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
設nA為阿伏加德羅常數的數值,下列說法正確的是
| A.1mol Cl2與過量的鎂鐵反應,轉移2nA個電子 |
| B.常溫下,16g CH4含有8nA個電子 |
| C.1L 0.5 mol·L-1Na2SO4溶液中含有nA個SO42- |
| D.常溫常壓下,22.4LCO2含有nA個CO2分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列溶液配制實驗的描述完全正確的是
| A.在容量瓶中先加入一定體積的水,再加入濃硫酸配制準確濃度的稀硫酸 |
| B.用濃鹽酸配制(體積比1:1)的稀鹽酸(約6mol.L-1)通常需要用容量瓶等儀器 |
| C.配制NH4Fe(SO4)2標準溶液時,加入一定量H2SO4以防水解 |
| D.用PH=1的鹽酸配制100mL,PH=2的鹽酸所需全部玻璃儀器有100mL容量瓶、燒杯、玻璃棒、膠頭滴管 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在標準狀況下,將V L A氣體(摩爾質量為M g·mol-1)溶于0.1 L水中,所得溶液的密度為ρ g·cm-3,則此溶液的物質的量濃度(mol·L-1)為
A. | B. |
C.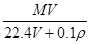 | D. |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
將15.6 g Na2O2和5.4 g Al同時放入一定量的水中,充分反應后得到200 mL溶液,再向該溶液中緩慢通入標準狀況下的HCl氣體6.72 L,若反應過程中溶液的體積保持不變,則下列說法正確的是
| A.標準狀況下,反應過程中得到7.84 L的氣體 |
| B.最終得到的溶液中c(Na+)=c(Cl-)+c(OH-) |
| C.最終得到7.8 g的沉淀 |
| D.最終得到的溶液中c(Na+)=1.5 mol·L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用NA表示阿伏加德羅常數的值。下列敘述正確的是
| A.25 ℃時,pH=12的Ba(OH)2溶液中含有的OH-數目為0.02NA |
| B.室溫下,14.0 g乙烯和丁烯的混合氣體中含有C—H鍵數目為2.0NA |
| C.1 L 0.5 mol·L-1的(NH4)2SO4溶液中含有的NH數目為NA |
| D.標準狀況下,22.4 L CCl4中含有共用電子對數目為4.0NA |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
設NA為阿伏加德羅常數的值。下列敘述正確的是
| A.在標況下,11.2 L NO與11.2 L O2混合后所含分子數為0.75NA |
| B.常溫常壓下,16 g O3所含的電子數為8NA |
| C.0.1 mol Na2O2晶體中含有0.4NA個離子 |
| D.鋁跟氫氧化鈉溶液反應生成1 mol氫氣時,轉移的電子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
三聚氰胺又名蛋白精[分子式:C3N3(NH2)3,相對分子質量:126]是一種低毒性化工產品,嬰幼兒大量攝入可引起泌尿系統疾患。有關三聚氰胺的下列說法正確的是 ( )。
| A.2.52 g三聚氰胺含氮原子數目為0.12NA |
| B.標準狀況下1 mol的三聚氰胺的體積為22.4 L |
| C.三聚氰胺含氮量約為10% |
| D.三聚氰胺的摩爾質量為126 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com