
【題目】下列有機物的命名正確的是
A.CH2=CH—CH=CH2 1,3-二丁烯
B.CH3CH2CH(CH3)OH 2-甲基-1-丙醇
C.![]() 2-甲基-3-丁炔
2-甲基-3-丁炔
D.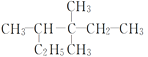 3,3,4-三甲基己烷
3,3,4-三甲基己烷
【答案】D
【解析】
烷烴的命名原則是:找出最長的碳鏈當主鏈,依碳數命名主鏈,前十個以天干(甲、乙、丙...)代表碳數,碳數多于十個時,以中文數字命名,如:十一烷;從最近的取代基位置編號:1、2、3...(使取代基的位置數字越小越好),以數字代表取代基的位置,數字與數字之間以“,”隔開,數字與中文數字之間以“-”隔開;有多個取代基時,以取代基數字最小且最長的碳鏈當主鏈,并依甲基、乙基、丙基的順序列出所有取代基;有兩個以上的取代基相同時,在取代基前面加入中文數字:一、二、三...,如:二甲基;如果含有官能團,則含有官能團的最長碳鏈作主鏈,編號也是從離官能團最近的一端開始,據此分析解答。
A.該物質是二烯烴,兩個雙鍵的位置在1,2號C原子和3,4號碳原子之間,因此名稱為1,3-丁二烯,A選項錯誤;
B.CH3CH2CH(CH3)OH的主鏈有4個碳,2號為羥基,因此名稱為2-丁醇,B選項錯誤;
C.![]() 屬于炔烴,最長碳鏈含有4個碳原子,離叁鍵最近一端編號,甲基在3號碳上,因此名稱為3-甲基-1-丁炔,C選項錯誤;
屬于炔烴,最長碳鏈含有4個碳原子,離叁鍵最近一端編號,甲基在3號碳上,因此名稱為3-甲基-1-丁炔,C選項錯誤;
D.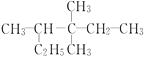 屬于烷烴,主鏈有6個碳,2個甲基位于3號碳原子上,1個甲基位于4號碳原子上,因此其名稱為3,3,4-三甲基己烷,D選項正確;
屬于烷烴,主鏈有6個碳,2個甲基位于3號碳原子上,1個甲基位于4號碳原子上,因此其名稱為3,3,4-三甲基己烷,D選項正確;
答案選D。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】已知反應S2O82-(aq)+2I-(aq)![]() 2SO42-(aq)+I2(aq),若往該溶液中加人含Fe3+的某溶液,反應機理:①2Fe3++(aq)+2I-(aq)
2SO42-(aq)+I2(aq),若往該溶液中加人含Fe3+的某溶液,反應機理:①2Fe3++(aq)+2I-(aq)![]() I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O82-(aq)
I2(aq)+2Fe2+(aq)②2Fe2+(aq)+S2O82-(aq) ![]() 2Fe3+(aq)+2SO42-(aq),下列有關該反應的說法不正確的是
2Fe3+(aq)+2SO42-(aq),下列有關該反應的說法不正確的是
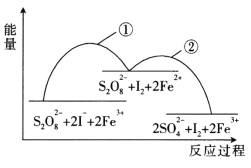
A.增大S2O82-濃度或I-濃度,反應①、反應②的反應速率均加快
B.Fe3+是該反應的催化劑
C.因為正反應的活化能比逆反應的活化能小,所以該反應是放熱反應
D.往該溶液中滴加淀粉溶液,溶液變藍,適當升溫,藍色加深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值,下列說法中正確的數目是
①12.0g熔融的NaHSO4中含有的陽離子數為0.2NA
②1mol Na2O 和Na2O2混合物中含有的陰、陽離子總數是3NA
③常溫常壓下,92g的NO2和N2O4混合氣體含有的原子數為6NA
④7.8g![]() 中含有的碳碳雙鍵數目為0.3NA
中含有的碳碳雙鍵數目為0.3NA
⑤用1L1.0 mol/LFeCl3溶液制備氫氧化鐵膠體,所得氫氧化鐵膠粒的數目為NA
⑥1mol SO2與足量O2在一定條件下充分反應生成SO3,共轉移2NA個電子
⑦在反應KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2轉移的電子數為5NA
⑧常溫常壓下,17 g甲基(-14CH3)中所含的中子數為9NA
A.3B.4C.5D.6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)可用于合成除草劑和殺蟲劑。一定條件下,恒容密閉容器中,發生反應H2S(g)+CO2(g) ![]() COS(g)+H2O(g),能充分說明該反應已經達到化學平衡狀態的是
COS(g)+H2O(g),能充分說明該反應已經達到化學平衡狀態的是
A. 正、逆反應速率都等于零
B. H2S、CO2、COS、H2O的濃度相等
C. H2S、 CO2、COS、H2O的濃度不再變化
D. H2S、CO2、COS、H2O在密閉容器中共存
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知4NH3+5O2=4NO+6H2O ,若反應速率分別用V(NH3)、 V(O2)、V(NO)、V(H2O)表示,則正確的關系是
A. ![]() V(NH3)=V(O2) B.
V(NH3)=V(O2) B. ![]() V(O2)=V(H2O)
V(O2)=V(H2O)
C. ![]() V(NH3)=V(H2O) D.
V(NH3)=V(H2O) D. ![]() V(O2)=V(NO)
V(O2)=V(NO)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗裝置不能達到實驗目的的是
A.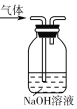 用裝置除去乙烯中的少量酸性氣體
用裝置除去乙烯中的少量酸性氣體
B.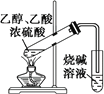 用裝置完成實驗室制取乙酸乙酯
用裝置完成實驗室制取乙酸乙酯
C. 用裝置證明溫度對化學平衡的影響
用裝置證明溫度對化學平衡的影響
D.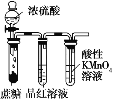 用裝置驗證濃硫酸具有脫水性、強氧化性,SO2具有漂白性、還原性
用裝置驗證濃硫酸具有脫水性、強氧化性,SO2具有漂白性、還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,在容積為2 L的密閉容器中,A、B的物質的量隨時間變化的曲線如圖所示,請據圖回答下列問題:
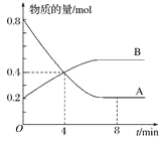
(1)該反應的化學方程式為_______________。
(2)在4 min末時,A、B的物質的量濃度c(A)________c(B),從0~4 min內A、B的物質的量濃度變化量Δc(A)________Δc(B)(以上填“>”、“<”或“=”)。
(3)反應開始至4 min時,A的平均反應速率為_______________________。
(4)4 min時,反應是否達到平衡狀態?________(填“是”或“否”)。8 min時,υ(正)________(填“>”、“<”或“=”)υ(逆)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫、容積為2L的密閉容器中通入1 mol X和2 mol Y,發生反應:X(g)+2Y(g)![]() M(g) ΔH=-a kJ/mol(a>0),5 min末測得M的物質的量為0.4 mol。則下列說法正確的是
M(g) ΔH=-a kJ/mol(a>0),5 min末測得M的物質的量為0.4 mol。則下列說法正確的是
A. 0~5 min,Y的平均反應速率為0.08 mol·L-1·min-1
B. 當容器中混合氣體密度不變時達到平衡狀態
C. 平衡后升高溫度,X的反應速率降低
D. 到達平衡狀態時,反應放出的熱量為a kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素A、B、C、D、E的原子序數依次增大,且均小于36。A的基態原子2p能級有3個單電子;C的基態原子2p能級有1個單電子;D的價電子數為2且與E同周期;E的基態原子的內部各能層均排滿,且4s能級有1個單電子。回答下列問題:
(1)基態E原子的價電子排布式為____________________
(2)A、B、C三種元素第一電離能由大到小的順序為___________(用元素符號表示)。
(3)與A的單質分子互為等電子體的分子和離子分別是________(用分子和離子符號表示)。AB2的空間構型為___________,其中A原子的雜化類型是_______________
(4)B元素簡單氫化物的沸點是同族元素中最高的,原因是_____________
(5)向含E元素的硫酸鹽溶液中加入過量氨水,可得到深藍色透明溶液。向溶液中加人乙醇,將析出深藍色晶體。該晶體的化學式為[Cu(NH3)4]SO4H2O晶體中陽離子的結構式為____________
(6)C和D形成化合物的晶胞結構如圖所示,已知晶體的密度為ρg/cm,阿伏加德羅常數為NA,則晶胞邊長a=______________cm(用含ρ、NA的計算式表示)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com