
【題目】對一定溫度下的恒容容器中的可逆反應A(g)+3B(g) ![]() 2C(g),下列敘述不能作為平衡標志的是( )
2C(g),下列敘述不能作為平衡標志的是( )
①C的生成速率與C的分解速率相等
②單位時間內生成amolA,同時生成3amolB
③A、B、C的濃度不再變化
④A、B、C的壓強不再變化
⑤混合氣體的總壓強不再變化
⑥混合氣體的物質的量不再變化
⑦A、C的物質的量之比不再變化
⑧A、B、C的分子數之比為1:3:2
A.②⑧ B.①⑥ C.②④ D.③⑧
【答案】A
【解析】
試題分析:①生成C的速率與C分解的速率相等,正逆反應速率相等,反應達到平衡狀態,①不選;②無論反應是否達到平衡狀態都存在單位時間內生成a molA同時生成3a molB,所以不能根據此來判斷平衡狀態,②選;③A、B、C的濃度不在變化時,正逆反應速率相等,該反應達到平衡狀態,③不選;④A、B、C的壓強不再變化說明反應達到平衡狀態,④不選;⑤該反應前后氣體計量數之和減小,混合氣體的總壓強不再變化時說明反應達到平衡狀態,⑤不選;⑥該反應前后氣體計量數之和減小,當混合氣體的物質的量不在變化時正逆反應速率相等,該反應達到平衡狀態,⑥不選;⑦A、C分別是反應物和生成物,二者的物質的量之比不再變化說明反應達到平衡狀態,⑦不選;⑧A、B、C的分子數之比為1:3:2,該反應不一定達到平衡狀態,與反應初始濃度及轉化率有關,所以不能據此判斷平衡狀態,⑧選;綜上所述,答案選A。


科目:高中化學 來源: 題型:
【題目】氯化二硫(S2Cl2)是廣泛用于橡膠工業的硫化劑,其分子結構如下圖所示。常溫下S2Cl2是一種橙黃色的液體,遇水易水解,并產生能使品紅褪色的氣體。下列說法錯誤的是( )

A.S2Cl2的結構式為Cl-S-S-Cl
B. S2Cl2為含有極性鍵和非極性鍵的非極性分子
C.S2Br2與S2Cl2結構相似,熔沸點:S2Br2>S2Cl2
D.S2Cl2與H2O反應的化學方程式可能為: 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有常見金屬A、B,它們之間存在如下的轉化關系(圖中有些反應的產物和反應的條件沒有全部標出),其中G、H為白色沉淀,C是最輕的氣體。請回答下列問題:
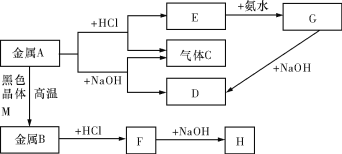
(1)寫出金屬A和物質D的名稱或化學式:________________、________________。
(2)寫出E轉化為G的離子方程式:_____________________。
(3)寫出H放在空氣中的現象:______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)聚丙烯腈纖維商品名叫腈綸,被稱為“人造羊毛”,其單體丙烯腈(C3H3N)可用“丙烯氨氧化法”生產,生成丙烯腈的熱化學方程式為:C3H6(g)+NH3(g)+3/2O2(g)=C3H3N(g)+3H2O(g) △H=-515kJ/mol該法在生產中有多種副產物生成,其中丙烯醛(C3H4O)是主要副產物之一。若氣態丙烯與氧氣反應生成11.2g氣態丙烯醛和水蒸汽,同時放出70.6kJ熱量,則反應的熱化學方程式為:___________,該反應在任何溫度下都能自發進行,其原因是_____________。
(2)圖(a)為在某一時間段一密閉體系中生成丙烯腈的反應速率與反應進程的曲線關系。由圖可知,t1時刻表示體系改變的反應條件為_________;t2時刻表示體系改變另一反應條件,此時平衡______移動(填“正向”、“逆向”或“不”)。
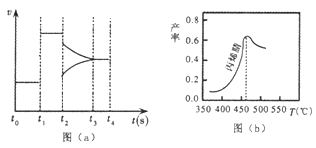
(3)圖(b)為丙烯腈產率與反應溫度的關系曲線,最高產率對應的溫度為460℃ 。在相同的反應時間內,高于460℃時丙烯腈產率降低的可能原因是_____(填序號)。
A.催化劑活性降低 B.平衡常數變大 C.副反應增多
D.反應活化能增大 E.平衡常數變小
在相同的反應時間內.低于460℃時丙烯腈的產率______(填“是”或“不是”)對應溫度下的平衡轉化率,判斷理由是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求完成下列各題:
(1)粘土[主要成分Al2Si2O5(OH)4] 是制備陶瓷的原料,請以氧化物形式表示粘土的組成_____________。
(2)現用四氯化硅和氮氣在氫氣中加強熱發生反應,可制得高純度氮化硅,反應的化學方程式為_________________________。
(3)雕花玻璃是用氫氟酸對玻璃進行刻蝕,這一過程中發生反應的化學方程式為_______。
(4)明礬可用于凈水,請說明原因________________________。
(5)下圖,若A、B、C中均含同一種常見金屬元素,該元素在C中以陰離子形式存在, B是白色膠狀沉淀。

①實驗室中常用A與某種溶液反應制備B,請寫出該反應的離子方程式 _________________。
②A與C也可以反應生成B,請寫出反應的離子方程式___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在298K和101kPa條件下,有如下反應:
反應Ⅰ:C(s) + O2(g) = CO2(g) △ H1=-393.5 kJ·mol-1
反應Ⅱ:2C(s) + O2(g) = 2CO(g) △ H2=-221 kJ·mol-1
反應Ⅲ:N2(g) + O2(g) = 2NO(g) △ H3=+180.5 kJ·mol-1
試回答下列問題:
(1)汽車尾氣凈化原理為反應Ⅳ:2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g) △ H=______,該反應能自發進行的條件是_______。(填“高溫”、“低溫”或“任意溫度”)。
N2(g) + 2CO2(g) △ H=______,該反應能自發進行的條件是_______。(填“高溫”、“低溫”或“任意溫度”)。
(2)如果在一定溫度下,體積為 2 升的密閉容器中發生化學反應Ⅳ,0~4min各物質物質的量的變化如下表所示:
物質(mol) 時間 | NO | CO | N2 | CO2 |
起始 | 0.40 | 1.0 | ||
2 min 末 | 2.0 | 0.80 | 1.6 | |
4 min 末 | 1.6 |
①求 0~2min 內用 CO 來表示的平均反應速率 v(CO)=________。
②試計算該溫度下反應Ⅳ 的化學平衡常數 K=_________。
(3)若一定溫度下,在容積可變的密閉容器中,上述反應Ⅳ達到平衡狀態,此時容積為3L, c(N2)隨時間 t 的變化曲線 x 如圖所示。
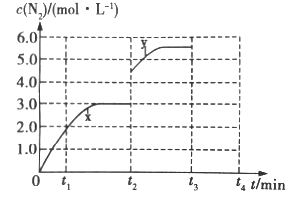
①若在 t2min時改變一個條件,c(N2)隨反應時間 t 的變化如曲線 y 所示,則改變的條件是______。
②若在t2min時升高溫度,t3min時重新達到平衡,請在圖中畫出在 t2~t4 內 c(N2)的變化曲線______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,有關說法不正確的是( )

A. 元素b的單質不能與酸性氧化物發生化學反應
B. a、b、d、f四種元素的離子半徑:f>d>a>b
C. 元素c的氧化物既能與酸反應又能與堿反應
D. a、c、e的最高價氧化物對應的水化物之間能夠相互反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等體積的NaCl、MgCl2、AlCl3三種溶液分別與等體積等物質的量濃度的AgNO3溶液恰好完全反應,則NaCl、MgCl2、AlCl3三種溶液的物質的量濃度之比是
A.1:2:3 B.3:2:1 C.6:3:2 D.1:1:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com