
核電荷數小于l8的某元素X,其原子的電子層數為n,最外層電子數為(2n+1),
原子核內質子數為(2n2一1)。下列關于元素X的說法中,不正確的是( )
| A.其最高化合價一定為+5 | B.可以形成化學式為KXO3的鹽 |
| C.其氫化物可以用來做噴泉實驗 | D.其最高價氧化物的水化物是強酸 |
A
解析試題分析:核電荷數小于l8的某元素X,其原子的電子層數為n,則1<n≤3,最外層電子數為(2n+1),最外層電子數小于8,原子核內質子數為(2n2-1),當n=2時,核內質子數是7,最外層電子數是5,符合條件,為N元素;如果n=3,核內質子數是17,最外層電子數是7,為Cl元素,符合條件,所以X可能是N或Cl元素。A、如果X是N元素,其最高正化合價為+5,如果是Cl元素,其最高正價為+7,錯誤;B、N或Cl元素都可以形成化學式為KXO3的鹽,如KNO3或KClO3,正確;C、氨氣或氯化氫都極易溶于水,所以都可以做噴泉實驗,正確;D、硝酸和高氯酸都是強酸,所以N或Cl元素的最高價氧化物的水化物是強酸,正確。
考點:本題考查原子結構和元素周期律。


科目:高中化學 來源: 題型:單選題
下列關于堿金屬元素和鹵素的說法中,錯誤的是( )
| A.隨核電荷數的增加,堿金屬元素和鹵素的原子半徑都逐漸增大 |
| B.堿金屬元素中,鋰原子失去最外層電子的能力最弱;鹵素中,氟原子得電子能力最強 |
| C.鉀與水的反應比鈉與水的反應更劇烈 |
| D.溴單質與水的反應比氯單質與水的反應更劇烈 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
根據下列事實:①X+Y2+=X2++Y;②Z+2H2O(冷水)=Z(OH)2+H2↑;③Z2+的氧化性比X2+弱;④由Y、W做電極組成的原電池,電極反應為W2++2e- =W,Y-2e- =Y2+。可知X、Y、W、Z的還原性由強到弱的順序是
| A.X>Z>Y>W | B.Z>W>X>Y | C.Z>X>Y>W | D.Z>Y>X>W |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某元素的一種同位素X的原子質量數為A,含N個中子,它與1H原子組成1HmX分子,在a g 1HmX中所含質子的物質的量是
A.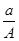 (A-N+m)mol (A-N+m)mol | B.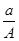 (A-N)mol (A-N)mol |
C.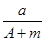 (A-N)mol (A-N)mol | D.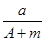 (A-N+m)mol (A-N+m)mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
原計劃實現全球衛星通訊需發射77顆衛星,這一數字與銥(Ir)元素的原子核外電子數恰好相等,因此稱為“銥星計劃”.已知銥的一種同位素的質量數為191,則其核內的中子數與質子數之差是
| A.77 | B.114 | C.37 | D.268 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
有A、B、X、Y四種短周期元素,其簡單離子A+、B2+、X-、Y2-的電子層結構相同。則下列比較中正確的的是( )
A.原子序數:A>B>X>Y B.離子半徑:A+ > B2+ > X- > Y2-
C.氫化物穩定性:H2Y > HX D.元素金屬性:A > B
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述中錯誤的是 ( )
| A.原子半徑Cl>S>O | B.還原性Na>Mg>Al |
| C.穩定性HF>HCl>HBr | D.酸性HClO4>H2SO4>H3PO4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com