
【題目】對工業廢水和生活污水進行處理是防止水體污染、改善水質的主要措施之一。
(1)硫酸廠的酸性廢水中砷(As)元素(主要以H3AsO3形式存在)含量極高,為控制砷的排放,某工廠采用化學沉淀法處理含砷廢水。請回答以下問題:
①已知砷是氮的同族元素,比氮原子多2個電子層,砷在元素周期表的位置為____________。
②工業上采用硫化法(通常用硫化鈉)去除廢水中的砷,生成物為難溶性的三硫化二砷,該反應的離子方程式為_____________________。
(2)電鍍廠的廢水中含有的CN-有劇毒,需要處理加以排放。處理含CN-廢水的方法之一是在微生物的作用下,CN-被氧氣氧化成HCO3-,同時生成NH3,該反應的離子方程式為_____________。
(3)電滲析法處理廚房垃極發酵液,同時得到乳酸的原理如圖所示(圖中“HA”表示乳酸分子,A-表示乳酸根離子):
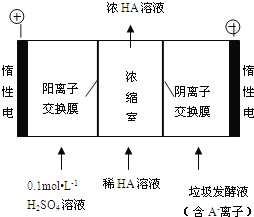
①陽極的電極反應式為________________________。
②簡述濃縮室中得到濃乳酸的原理:________________________。
③電解過程中,采取一定的措施可控制陽極室的pH約為6~8,此時進入濃縮室的OH-可忽略不計。400 mL 10 g/L 乳酸溶液通電一段時間后,濃度上升為145 g/L(溶液體積變化忽略不計),陰極上產生的H2在標準狀況下的體積約為________L(提示:乳酸的摩爾質量為90 g/mol)。
【答案】第四周期第ⅤA族2H3AsO3+3S2-+6H+═As2S3↓+6H2O4H2O+2CN-+O2═2HCO3-+2NH32H2O-4e-═4H++O2↑陽極H2O放電,c(H+)增大,H+從陽極通過陽離子交換膜進入濃縮室,A-從陰極通過陰離子交換膜進入濃縮室,H++A-═HA,乳酸濃度增大6.72
【解析】
(1)①砷原子電子層數=周期數=4,最外層電子數=族序數=5,所以砷位于第四周期第ⅤA族;因此本題答案是:第四周期第ⅤA族。
②根據信息:硫化鈉可以和廢水中的砷反應,生成難溶性的三硫化二砷,據此得到反應的離子方程式為:2H3AsO3+3S2-+6H+═As2S3↓+6H2O;因此,本題答案是:2H3AsO3+3S2-+6H+═As2S3↓+6H2O。
(2)CN-被氧氣氧化成HCO3-,同時生成NH3,該反應的離子方程式為:4H2O+2CN-+O2═2HCO3-+2NH3;因此,本題答案是:4H2O+2CN-+O2═2HCO3-+2NH3。
(3) ①陽極上是氫氧根離子失電子發生氧化反應,電極反應式為:2H2O-4e-═4H++O2↑ ;因此本題答案是:2H2O-4e-═4H++O2↑。
②在電解池的陽極上是氫氧根放電,所以c(H+)增大,并且H+從陽極通過陽離子交換膜進入濃縮室;根據電解原理,電解池中的陰離子移向陽極,即 A-通過陰離子交換膜從陰極進入濃縮室,發生反應:H++A-═HA,使乳酸濃度增大;綜上所述,本題答案是:陽極H2O放電,c(H+)增大,H+從陽極通過陽離子交換膜進入濃縮室,A-從陰極通過陰離子交換膜進入濃縮室,H++A-═HA,乳酸濃度增大。
③在陽極上發生電極反應:4OH—-4e-=2H2O+O2↑,陰極上發生電極反應:2H++2e-=H2↑,根據電極反應方程式,則有:HA—H+--1/2H2,據差值法,乳酸的濃度變化量是(145-10)/90=1.5mol/L,即生成HA的物質的量是1.5×0.4=0.6mol,即產生氫氣0.3mol,即0.3×22.4=6.72L;綜上所述,本題答案是:6.72L。


科目:高中化學 來源: 題型:
【題目】某班同學用如下實驗探究Fe2+、Fe3+的性質。請回答下列問題:
(1)甲組同學取l0mL0.l mol·L-1KI溶液,加入6 mL0.l mol·L-1 FeCl3溶液混合。分別取2 mL此溶液于3支試管中進行如下實驗:
①第一支試管中加入lmLCCl4充分振蕩、靜置, CCl4層顯紫色;
②第二支試管中加入1滴K3[Fe(CN)6]溶液,生成藍色沉淀:
③第三支試行中加入1滴KSCN溶液,溶液變紅。
實驗②檢驗的離子是(填離子符號) ______________;實驗①和③說明:在I-過量的情況下,溶液中仍含有(填離子符號)_______________,由此可以證明該氧化還原反應為___________________(填可逆反應或不可逆反應)。
(2)乙組同學向盛有H2O2溶液的試管中加入幾滴酸化的FeCl2溶液,溶液變成棕黃色,發生反應的離子方程式為____________________________;一段時間后,溶液中有氣泡出現,并放熱,隨后有紅褐色沉淀生成。產生氣泡的原因是__________________________________;生成沉淀的原因是(用平衡移動原理解釋)_________________________________________________。
(3)丙組同學模擬工業上用NaClO3氧化酸性FeCl2廢液制備FeCl3。
①若酸性FeCl2 廢液中:c(Fe2+)=2.0×10-2 mol·L-1,c(Fe3+)=1.0×10-3 mol·L-1,c(Cl-)=5.3×10-2 mol·L-1,則該溶液的pH約為_____________。
②完成NaClO3氧化FeCl2的離子方程式:□ClO3-+□Fe2++□________=□Cl-+□Fe3++□________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知C(s,石墨)=C(s,金剛石) H>0,下列判斷正確的是( )
A.此反應為放熱反應
B.斷裂1mol石墨的化學鍵需要吸收的能量小于生成1mol金剛石化學鍵所放出的能量
C.石墨比金剛石穩定
D.此變化為物理變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將純鋅片和純銅片按圖示方式插入同濃度的稀硫酸中一段時間。以下敘述正確的是( )

A. 兩燒杯中銅片表面均有氣泡產生
B. 甲燒杯中的電流與陽離子流向均為Zn→Cu
C. 兩燒杯中溶液的pH均增大
D. 兩燒杯在相同時間內轉移電子數相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酚酞的結構簡式如圖,下列關于酚酞的說法一定正確的是
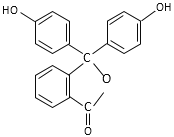
A. 酚酞的分子式是C20H12O4
B. 分子中的碳原子不在同一平面
C. 1 mol酚酞最多可消耗2 mol NaOH
D. 常溫下,由水電離的c(H+)=10-13mol·L-1的溶液中滴入酚酞試液后,溶液呈紅色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質性質的變化規律與分子間作用力有關的是( )
A.HF、HCl、HBr、HI的熱穩定性依次減弱
B.金剛石的硬度大于硅,其熔、沸點也高于硅
C.NaF、NaCl、NaBr、Nal的熔點依次降低
D.F2、Cl2、Br2、I2的熔、沸點逐漸升高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫化鋁鋰(LiAlH4)是有機合成中的重要還原劑。某課題組設計實驗制備氫化鋁鋰并測定其純度。已知:氫化鋁鋰、氫化鋰遇水都劇烈反應并產生同一種氣體。活潑金屬硫化物與酸反應產生H2S氣體。
Ⅰ、制備氫化鋰:選擇下圖中的裝置制備氫化鋰(有些裝置可重復使用):

(1)裝置的連接順序(從左至右)為A→___________________________________。
(2)檢查好裝置的氣密性,打開裝置A中分液漏斗的活塞后,點燃酒精燈前需進行的實驗操作是________。
Ⅱ、制備氫化鋁鋰
1947年,Schlesinger、Bond和Finholt首次制得氫化鋁鋰,其方法是使氫化鋰與無水三氯化鋁按一定比例在乙醚中混合,攪拌,充分反應后,經一系列操作得到LiAlH4晶體。
(3)寫出氫化鋰與無水三氯化鋁反應的化學方程式_________________________。
Ⅲ.測定氫化鋁鋰產品(不含氫化鋰)的純度
(4)按下圖連接好裝置后,檢查裝置氣密性的操作是:_____________________。裝好藥品(Y形管中的蒸餾水足量,為了避免氫化鋁鋰遇水發生爆炸,蒸餾水中需摻入四氫呋喃作稀釋劑),啟動反應的操作是__________________。

(5)在標準狀況下,反應前量氣管(由堿式滴定管改裝而成)讀數為V1 mL,反應完畢并冷卻之后,量氣管讀數為V2 mL。該樣品的純度為_________(用含a、V1、V2的代數式表示)。如果起始讀數時俯視刻度線,測得的結果將_________(填“偏高”“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)反應A+B→C(放熱)分兩步進行①A+B→X(吸熱);②X→C(放熱)。下列示意圖中,能正確表示總反應過程中能量變化的是_____。

(2)合成氨工業中,合成塔中每產生2mol NH3,放出92.2kJ熱量,已知(見圖):則1mol N﹣H鍵斷裂吸收的能量約等于_____kJ。

(3)請將 Zn+2Ag+=2Ag+Zn2+設計成原電池,并畫出簡易裝置圖,并注明電極材料以及電解質溶液___。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com