
下面是人們對于化學科學的各種常見認識,其中錯誤的是( )。
| A.化學將在能源、資源的合理開發和安全應用方面大顯身手 |
| B.化學是在被運用于破壞環境而沒有治理環境污染 |
| C.化學是一門具有極強實用性的科學 |
| D.化學是一門以實驗為基礎的自然科學 |
 鷹派教輔銜接教材河北教育出版社系列答案
鷹派教輔銜接教材河北教育出版社系列答案 初中暑期銜接系列答案
初中暑期銜接系列答案科目:高中化學 來源: 題型:單選題
下列有關工業生產敘述正確的是
| A.工業上通常使用電解法制備金屬鈉、鎂、鋁等 |
| B.合成氨工業中,將NH3及時液化分離有利于加快反應速率 |
| C.硫酸工業中,采用常壓條件的原因是此條件下催化劑活性最高 |
| D.電解精煉銅時,將粗銅與電源的負極相連 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨是一種重要的化工原料,氨的合成和應用是當前的重要研究內容之一。
(1)傳統哈伯法合成氨工藝中相關的反應式為: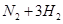


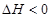 。
。
①該反應的平衡常數K的表達式為:K=_________。升高溫度,K值________(填“增大”“減小”或“不變”)。
②不同溫度、壓強下,合成氨平衡體系中NH3的物質的量分數見下表(N2和H2的起始物質的量之比為1:3)。分析表中數據,__________(填溫度和壓強)時H2轉化率最高,實際工業生產不選用該條件的主要原因是________________。
③下列關于合成氨說法正確是___________(填字母)
A. 使用催化劑可以提高氮氣的轉化率
B. 尋找常溫下的合適催化劑是未來研究的方向
C. 由于△H<0、△S>0,故合成氨反應一定能自發進行
(2)最近美國Simons等科學家發明了不必使氨先裂化為氫就可直接用于燃料電池的方法。它既有液氫燃料電池的優點,又克服了液氫不易保存的不足。其裝置為用鉑黑作為電極,加入電解質溶液中,一個電極通人空氣,另一電極通入氨氣。其電池反應為
你認為電解質溶液應顯______性(填“酸性”、“中性”、“堿性”),寫出負極電極反應式________。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
2013年度諾貝爾化學獎再次授予計算化學領域的科學家。以下基于結構理論進行繁難計算得出的是
| A.天然氣的熱值 | B.合成氨的原子利用率 |
| C.尿素的含氮量 | D.p軌道電子云的形狀 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
關于假說有如下表述其中正確的是( )
| A.假說是對現實中已知事物或現象的一種簡化處理 |
| B.假說是對未知領域的事物或現象提出的一種推測 |
| C.假說是對一個問題的所有幻想和假定 |
| D.假說最終都可以變成科學理論 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鈦冶煉廠與氯堿廠、甲醇廠組成一個產業鏈(如圖所示),將大大提高資源的利用率,減少環境污染。
請回答下列問題:
(1)Ti的原子序數為22,Ti位于元素周期表中第_______周期,第______族。
(2)寫出鈦鐵礦在高溫下與焦炭經氯化得到四氯化鈦的化學方程式 。
(3)制備TiO2的方法之一是利用TiCl4水解生成TiO2·x H2O,再經焙燒制得。水解時需加入大量的水并加熱,請結合化學方程式和必要的文字說明原因: 。
(4)由TiCl4→Ti 需要在Ar氣中進行的理由是_________________________________。反應后得到Mg、MgCl2、Ti的混合物,可采用真空蒸餾的方法分離得到Ti,依據下表信息,需加熱的溫度略高于 ℃即可。
| | TiCl4 | Mg | MgCl2 | Ti |
| 熔點/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸點/℃ | 136.4 | 1090 | 1412 | 3287 |
 CH3OH(g)。若不考慮生產過程中物質的任何損失,上述產業鏈中每合成6mol甲醇,至少需額外補充H2 mol。
CH3OH(g)。若不考慮生產過程中物質的任何損失,上述產業鏈中每合成6mol甲醇,至少需額外補充H2 mol。查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
農業生產中使用最廣泛的磷肥是過磷酸鈣,其主要成分是 (填化學式);在實際使用中,其不能與草木灰混合施用的原因是(用離子方程式表示) 。目前常用的濕法磷肥生產工藝是用硫酸分解磷礦石(主要成分為Ca5(PO4)3F),這樣處理的主要目的是 。
該生產工藝的有關反應為:
2Ca5(PO4)3F+7H2SO4=Ca3(PO4)2+4H3PO4+7CaSO4+2HF
Ca3(PO4)2+4H3PO4=3Ca(H2PO4)2
生成的氟化氫會和磷礦中帶入的二氧化硅反應生成SiF4,若直接排放到空氣中,將嚴重污染環境。某磷肥廠改進工藝,在吸收塔中將SiF4經水吸收后轉化為氟硅酸(H2SiF6)溶液和硅膠(SiO2),實現氟的循環使用和硅膠的合理利用,以減小對環境的污染,同時創造經濟效益。工藝流程如下:
(1)寫出吸收塔中反應的化學方程式____ 。
(2)該工藝流程中,設計兩個吸收塔的目的是 。
(3)氟硅酸與磷酸鈣和水反應可生成磷酸二氫鈣,原理是:
2H2SiF6+Ca3(PO4)2+4H2O=2CaSiF6·2H20 +Ca(H2PO4)2
CaSiF6·2H2O+2H2O=CaF2·SiO2·2H2O+4HF
4HF+Ca3(PO4)2=2CaF2+Ca(H2PO4)2
若利用氟硅酸與磷酸鈣和水反應代替硫酸與磷酸鈣反應生產Ca(H2PO4)2,理論上lkg氟硅酸可替代_____kg硫酸。
(4)分離得到的硅膠中因含有H2SiF6而稱含氟硅膠,含氟硅膠中SiO2易溶于沸騰的氟化銨溶液,得到(NH4)2SiF6溶液,此反應為可逆反應,加入氨水后,二氧化硅重新析出。寫出SiO2與氟化銨反應的化學方程式______ __。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.2Na+2H2O=2NaOH+H2↑ | B.Cl2+H2O=HCl+HClO |
| C.2F2+2H2O=4HF+O2 | D.CaO+H2O=Ca(OH)2 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.N2O4中,N的化合價為+4 |
| B.此反應中,偏二甲肼做還原劑 |
| C.此反應中,N2O4失去電子 |
| D.此反應中,R的分子式為C2H8N2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com