
���}Ŀ���Dʾ�������ڱ��еĎN������Ԫ�أ������f�����e�`���ǣ���
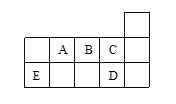
A. ED4�����и�ԭ�Ӿ��M��8��ӷ�(w��n)���Y(ji��)��(g��u)
B. AD3��ED4�ɷ��ӵ�����ԭ�Ӿ���sp3�s��
C. C��D��B(t��i)�仯�ﷀ(w��n)���ԏ�(qi��ng)����C��D
D. A��B��C�ؓ(f��)�Դ�С����C��A��B
���𰸡�D
��������
����(j��)Ԫ�������ڱ��е�λ��֪��A��B��C��D��E�քe��N��O��F��Cl��SiԪ�أ�
A��SiCl4������Si�Ļ��σr��+4�r��Cl�Ļ��σr��-1�r��Siԭ���������Ӕ�(sh��)��4��Clԭ���������Ӕ�(sh��)��7���t��ԭ�Ӷ��_(d��)����8��ӷ�(w��n)���Y(ji��)��(g��u)����A���_��
B��NCl3��SiCl4�ɷ��ӵ�����ԭ�Ӄr����ӌ���(sh��)����4�����Ծ���sp3�s������B���_��
C��Ԫ�صķǽ�����Խ��(qi��ng)�����B(t��i)�仯��Խ��(w��n)�����ǽ�����F>Cl������C��D��B(t��i)�仯�ﷀ(w��n)���ԏ�(qi��ng)����C>D����C���_��
D��Ԫ�طǽ�����Խ��(qi��ng)�ؓ(f��)��Խ��(qi��ng)��ͬ����Ԫ���S��ԭ����(sh��)����ǽ���������(qi��ng)�������ؓ(f��)�Դ�С����C��B��A����D�e�`��
���xD��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����Ќ�(sh��)�������F(xi��n)��ͽY(ji��)Փ�����_����
�x� | ���� | �F(xi��n)�� | �Y(ji��)Փ |
A | ������Q�Aһ�K�X���ھƾ������Ɵ� | �X���ۻ������� | �����X�����c(di��n)�^�� |
B | �������c��Һ�еμ������}�ᣬ���a(ch��n)���Ě��wͨ��Ʒ�t��Һ | Ʒ�t��Һ��ɫ | �ǽ����ԣ� |
C | ����ɰ����ȥ���o(h��)Ĥ���VƬ���XƬ����С���Π���ͬ�����քe����ͬ��ȵ�ϡ������ | �VƬ����a(ch��n)���������ʴ����XƬ | ߀ԭ�ԣ� |
D | �����£����ɸ���С��ͬ���Fᔷքe����������ϡ������ | �������Пo���@�F(xi��n)��ϡ�����Юa(ch��n)������ | ϡ����������Աȝ����Ꮚ(qi��ng) |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�������Ƶ��Ț�ĸ�������(y��ng)�У���Ԫ�ؼȱ������ֱ�߀ԭ����
A.2KClO3��I2=2KIO3��Cl��
B.Ca(ClO)2��4HCl=CaCl2��2Cl2����2H2O
C.4HCl��O2 ![]() 2Cl2��2H2O
2Cl2��2H2O
D.2NaCl��2H2O ![]() 2NaOH��H2����Cl2��
2NaOH��H2����Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���ķN������Ԫ��X��Y��Z��W�����ڱ��е�λ����D��ʾ��ԭ����(sh��)֮�͞�48�������f�������_����
X | Y | |
Z | W |
A.ԭ�Ӱ돽��r����С���^��![]()
B.X��Y���γɹ��r������XY��![]() �Ȼ�����
�Ȼ�����
C.Y�ķǽ����Ա�Z�ď�(qi��ng)������Y����߃r�������ˮ�������Դ���Z
D.Z����̓r�κ���x�ӵ�ʧ���������W�ď�(qi��ng)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�������f�������_����
A.![]() �����ЙC(j��)�����Ƿ�늽��|(zh��)
�����ЙC(j��)�����Ƿ�늽��|(zh��)
B.ʯ���ѻ����ѽ��Ŀ�ľ��Ǟ��ˌ��L期N�D(zhu��n)�����期N
C.ú�Ě⻯��Һ�����s���ǻ��W(xu��)׃��
D.���|(zh��)������ϩ����ϩ�քe���ȼ����������������|(zh��)����һ�Ӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��ȡһ���|(zh��)����![]() ��
��![]() ���w�Ļ���������m����ˮ����������Һ�ȷֳɃɷݣ�������һ���о�����μ���ij��ȵ��}�ᣬ�a(ch��n)���Ě��w�w�e�c�����}���w�e֮�g���P(gu��n)ϵ��D��ʾ������һ���м����^����
���w�Ļ���������m����ˮ����������Һ�ȷֳɃɷݣ�������һ���о�����μ���ij��ȵ��}�ᣬ�a(ch��n)���Ě��w�w�e�c�����}���w�e֮�g���P(gu��n)ϵ��D��ʾ������һ���м����^����![]() ��Һ���õ���ɫ����3.94g��ԇ�ش����І��}��
��Һ���õ���ɫ����3.94g��ԇ�ش����І��}��
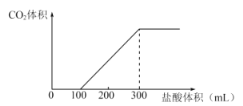
��1���}������|(zh��)������Ȟ�________________��
��2�����w�������![]() ���|(zh��)����________________��
���|(zh��)����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
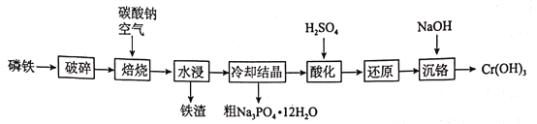
���}Ŀ�����F����P��Fe��Cr�ȣ����������a(ch��n)�^���Юa(ch��n)���ĸ��a(ch��n)�һ�N�����F��ԭ���Ƃ�![]() ��
��![]() ��������D��ʾ��
��������D��ʾ��
��֪��ˮ������Һ����Ҫ�ɷ֞�![]() ��
��![]() ��
��![]() ��
��![]() �ش����І��}��
�ش����І��}��
��1������������Ŀ�Ğ�________________________________________________________��
��2�����������r����(y��ng)��ԭ�ϼӵ�________����У������մ����������������ԭ����_____________���Y(ji��)�ϻ��W(xu��)����ʽ��ጣ���Cr���|(zh��)�l(f��)������Ҫ����(y��ng)�Ļ��W(xu��)����ʽ��________��
��3���M(j��n)һ���ἃ�������c���w�ķ�����________________��
��4�����ữ���r�l(f��)������(y��ng)���x�ӷ���ʽ��________________________________________________��
��5�������t���r����NaOH�{(di��o)��(ji��)��pH��________�r���t�x�ӄ��ó�����ȫ������֪��![]() ���x�ӝ�Ȟ�10-5mol/L�r���J(r��n)��ԓ�x�ӳ�����ȫ��
���x�ӝ�Ȟ�10-5mol/L�r���J(r��n)��ԓ�x�ӳ�����ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����1������ȼ��늳���ָ����������������W(xu��)���D(zhu��n)������ܵ��b�á�ij����ȼ��늳صĹ���ԭ����D��ʾ��
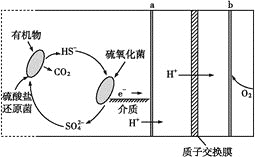
HS-�����������������D(zhu��n)����SO![]() �ķ���(y��ng)ʽ��__��
�ķ���(y��ng)ʽ��__��
��2��PbSO4�ἤ��늳ؿ������������(d��o)���Ĺ����Դ�������Y(ji��)��(g��u)��D��ʾ����������늽��|(zh��)�ğoˮLiCl��KCl�ܟ����ں�늳ؼ���˲�gݔ����ܡ�ԓ늳ؿ�����(y��ng)��PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb��
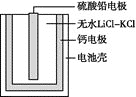
�ٷ���^���У�Li+��__(����ؓ(f��)�O���������O��)�Ƅӡ�
��ؓ(f��)�O����(y��ng)ʽ��__��
���·��ÿ�D(zhu��n)��0.2mol��ӣ���Փ������__gPb��
��3������ȼ��늳ؾ��кܴ�İl(f��)չ?ji��)���������ȼ��늳ع���ԭ����D��ʾ��
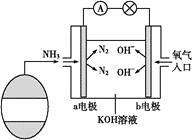
��a늘O��늘O����(y��ng)ʽ��__��
��һ�Εr�g�������b�����a(b��)��KOH��Ո����(j��)����(y��ng)ԭ�����ԭ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���������b��������P(gu��n)��(sh��)���������ǣ�������
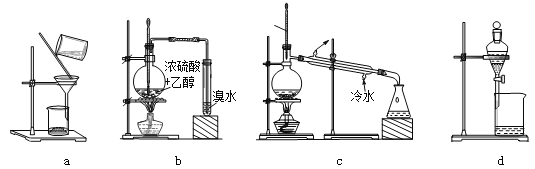
A. ��a�ß��^�V�ἃ������B. ��b�Ƃ䲢�z���ϩ
C. ��c��ȥ�屽�еı�D. ��d���x�������cˮ
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com