
【題目】下列實驗中,對于雜質(括號中的物質為雜質)的檢驗和除雜方法均正確的是
選項 | 目標物質和雜質 | 檢驗方法 | 除雜方法 |
A | FeCl2(FeCl3) | 滴入KSCN | 通入過量氯氣 |
B | NaCl(NH4Cl) | 加熱 | 加熱 |
C | KNO3(NaCl) | 焰色反應(透過藍色鈷玻璃) | 重結晶 |
D | Cl2(HCl) | 通入AgNO3溶液 | 通入飽和NaCl溶液中 |
科目:高中化學 來源: 題型:
【題目】下列圖示中,A為一種常見的單質,B、C、D、E是含A元素的常見化合物,它們的焰色反應均為黃色。
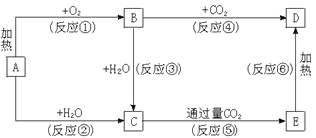
請填寫下列空白:
(1)C的電子式______________,B的電子式______________,D的化學式_______________。
(2)以上反應中屬于氧化還原反應的有____________________(填寫編號)。
(3)寫出B→D的化學方程式___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學——選修5:有機化學基礎】
有機物G(分子式為C13H18O2)是一種香料,如圖是該香料的一種合成路線。
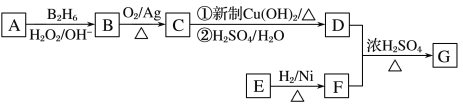
已知:
①E能發生銀鏡反應,在一定條件下,1 mol E能與2 mol H2反應生成F;
②R—CH===CH2  R—CH2CH2OH;
R—CH2CH2OH;
③有機物D的摩爾質量為88 g·mol-1,其核磁共振氫譜有3組峰;
④有機物F是苯甲醇的同系物,苯環上只有一個無支鏈的側鏈。
回答下列問題:
(1)用系統命名法命名有機物B________________。
(2)E的結構簡式為__________________________。
(3)C與新制Cu(OH)2反應的化學方程式為________________________________________。
(4)已知有機物甲符合下列條件:①為芳香族化合物;②與F互為同分異構體;③能被催化氧化成醛。符合上述條件的有機物甲有________種,寫出一種滿足苯環上有3個側鏈,且核磁共振氫譜有5組峰,峰面積比為6:2:2:1:1的有機物的結構簡式____________________。
(5)以丙烯等為原料合成D的路線如下:
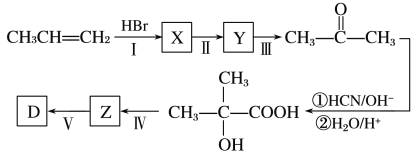
X的結構簡式為_______,步驟Ⅱ的反應條件為___________,步驟Ⅳ的反應類型為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅及其化合物在工業上有許多用途。回答下列問題:
(1)某工廠以輝銅礦(主要成分為Cu2S,含少量Fe2O3、SiO2等雜質)為原料制備不溶于水的堿式碳酸銅的流程如下:
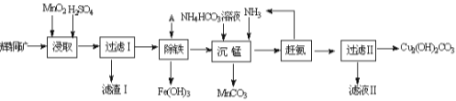
①浸取反應中氧化劑的化學式為_______;濾渣Ⅰ的成分為MnO2、S和_________(寫化學式)。
②“除鐵”這一步反應在25℃進行,加入試劑A調節溶液PH為4后,溶液中銅離子最大濃度不超過__________mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
③“沉錳”(除Mn2+)過程中反應的離子方程式__________________________ 。
④ 濾液Ⅱ經蒸發結晶得到的鹽主要是____________________ (寫化學式)。
(2)某實驗小組同學用電化學原理模擬濕法煉銅,進行了一系列探究活動。
①如下左圖為某實驗小組設計的原電池裝置,鹽橋內裝載的是足量用飽和氯化鉀溶液浸泡的瓊脂,反應前,電極質量相等,一段時間后,兩電極質量相差6.00 g,則導線中通過了________mol電子,若不考慮甲、乙兩池電解質溶液中的離子向鹽橋中移動,則甲、乙兩池電解質溶液的總質量與實驗開始前的電解質溶液的總質量相差__________g
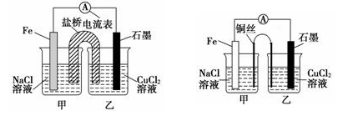
②其他條件不變,若將鹽橋換成光亮的U形彎銅絲浸入甲池與乙池,如上右圖所示,電流計指針偏轉方向與先前一樣,但偏轉角度明顯減小。一段時間后,乙池石墨棒浸入液面以下部分也析出了一層紫紅色固體,則甲池銅絲附近溶液的pH________(填“減小”、“增大”或“不變”) ,乙池中石墨為________極(填“正”、“負”、“陰”或“陽”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋中有豐富的食品、礦產、能源、藥物和水產資源等。下列有關說法正確的是
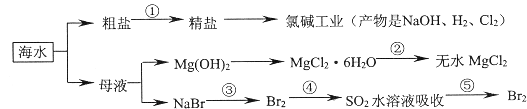
A.以NaCl為工業原料可以生產燒堿、純堿以及漂白粉等含氯產品
B.工業上通過電解飽和MgCl2溶液制取金屬鎂
C.第③④⑤步的目的是濃縮、富集溴單質,這三步中溴元素均被氧化
D.過程①除去粗鹽中的SO42-、Ca2+、Mg2+等雜質,加入的藥品順序為Na2CO3溶液→NaOH溶液→BaCl2溶液→過濾后加鹽酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗能成功的是( )
A. 將乙酸和乙醇混合加熱制乙酸乙酯
B. 苯和濃溴水反應制溴苯
C. 向濃苯酚中加幾滴稀溴水觀察沉淀
D. 用CuSO4溶液和過量NaOH溶液混合,然后加入幾滴乙醛,加熱煮沸觀察紅色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情況如下圖所示。沉淀的生成與溶解的pH列于下表。以下推斷正確的是
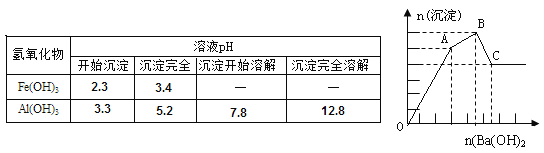
A.AB段可能發生的反應是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
B.C點的沉淀為Fe(OH)3
C.OA段可能發生的反應是:3Ba2++6OH-+3SO42-+Fe3++Al3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.據圖計算原溶液中c(Cl-)>c(SO42-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(Ⅰ)甲醇是一種新型的汽車動力燃料,工業上可通過CO和H2化合來制備甲醇。已知某些化學鍵的鍵能數據如下表:
化學鍵 C—C C—H H—H C—O ![]() H—O
H—O
鍵能/kJ·mol-1 348 413 436 358 1 072 463
請回答下列問題:
(1)已知CO中的C與O之間為叁鍵連接,則工業制備甲醇的熱化學方程式為 。
(2)某化學研究性學習小組模擬工業合成甲醇的反應,在容積固定為2 L的密閉容器內充入1 mol CO和2 mol H2,加入合適催化劑(體積可以忽略不計)后在250 ℃開始反應,并用壓力計監測容器內壓強的變化如下:

則從反應開始到20 min時,以CO表示的平均反應速率= ,該溫度下平衡常數K= ,若升高溫度則K值 (填“增大”、“減小”或“不變”)。
(3)下列描述中能說明上述反應已達平衡的是 。
A.2v(H2)正=v(CH3OH)逆
B.容器內氣體的平均摩爾質量保持不變
C.容器中氣體的壓強保持不變
D.單位時間內生成n mol CO的同時生成2n mol H2
(Ⅱ)回答下列問題:
(1)體積均為100 mL pH=2的CH3COOH與一元酸HX,加水稀釋過程中pH與溶液體積的關系如圖所示,則Ka(HX) Ka(CH3COOH)(填“>”、“<”或“=”)。
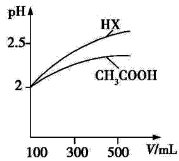
(2)25 ℃時,CH3COOH與CH3COONa的混合溶液,若測得pH=6,則溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精確值)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上制備相關物質,涉及的反應原理及部分流程較為合理的是
A. 制取鎂:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 冶煉鋁:鋁土礦![]() NaAlO2
NaAlO2![]() 無水AlCl3
無水AlCl3![]() Al
Al
C. 制溴:濃縮海水![]() Br2
Br2![]() HBr(aq)
HBr(aq) ![]() Br2
Br2
D. 制碘:海帶![]() 海帶灰
海帶灰![]() I2(aq)
I2(aq) ![]() I2
I2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com