
【題目】W、X、Y、Z是原子序數依次增大的四種短周期元素。n、p、r是由這些元素組成的二元化合物。m 是元素W的單質。q是元素Y的單質且是制作太陽能電池的原料。p在常溫下為常見無色液體,0.010mol·L-1的r溶液中c(H+)為0.010 mol·L-1,s是弱酸且不溶于水。上述物質的轉化關系如圖所示。下列說法不正確的是

A.r易溶于p
B.原子半徑:Z<Y
C.最高價氧化物對應水化物的酸性:Y<Z
D.最簡單氫化物的穩定性:X<Y
 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列敘述正確的是
A. 所含共價鍵數均為0.4NA的白磷(P4)和甲烷的物質的量相等
B. 1 mol Na與O2反應,生成Na2O和Na2O2的混合物共失去NA個電子
C. 1mol Na2O2固體中含有離子總數為4NA
D. 25℃時,pH=13的氫氧化鈉溶液中約含有NA個氫氧根離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列氮原子的電子排布圖表示的狀態中,能量由低到高的順序是_______(填字母代號)。

(2)P4S3可用于制造火柴,其分子結構如圖所示。
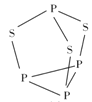
①P4S3分子中硫原子的雜化軌道類型為_______________。
②每個P4S3分子中含有的孤電子對的數目為__________________。
(3)科學家合成了一種陽離子“N5n+,其結構是對稱的,5個N排成"V"形,每個N都達到8電子穩定結構,且含有2個氮氮三鍵;此后又合成了一種含有“N5n+”的化學式為”N8”的離子晶體,其電子式為_________________。分子(CN)2中鍵與鍵之間的夾角為180°,并有對稱性,分子中每個原子的最外層均滿是8電子穩定結構,其結構式為_____。
(4)直鏈多磷酸根陰離子是由兩個或兩個以上磷氧四面體通過共用頂角氧原子連接起來的,如圖所示。則由n個磷氧四面體形成的這類磷酸根離子的通式為_________________。
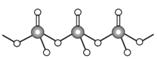
(5)碳酸鹽中的陽離子不同,熱分解溫度就不同。下表為四種碳酸鹽的熱分解溫度和金屬陽離子半徑
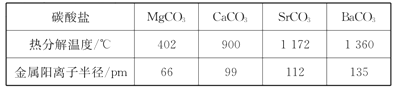
隨著金屬陽離子半徑的增大,碳酸鹽的熱分解溫度逐步升高,原因是_______________。
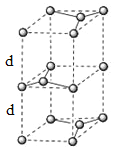
(6)石墨的晶體結構和晶胞結構如下圖所示。已知石墨的密度為pgcm3,C—C鍵的鍵長為![]() cm,阿伏加德羅常數的值為NA,則石墨品體的層間距為_________cm。
cm,阿伏加德羅常數的值為NA,則石墨品體的層間距為_________cm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知草酸受熱發生分解反應:H2C2O4![]() H2O+CO↑+CO2↑,某化學興趣小組為驗證草酸分解產物,設計如下實驗:
H2O+CO↑+CO2↑,某化學興趣小組為驗證草酸分解產物,設計如下實驗:

(1)按圖連接好裝置,檢查氣密性的方法是:_________________________________。
(2)實驗中B中現象是:______________。
(3)已知C和E中裝的是足量同種溶液,寫出離子反應方程式:_________________。
(4)實驗進行時D中黑色固體會逐漸變成紅色。寫出化學反應方程式:________________。
(5)實驗過程中會有分解產生的氣體經過D而未發生反應,采用F進行收集并測量氣體體積,讀數應注意____________________以便準確讀出常壓下的氣體體積。
(6)某同學查資料了解到有如下反應:CO+PdCl2+H2O=CO2+Pd↓+2HCl,于是建議將濃硫酸換成PdCl2溶液并撤去D及后面的裝置,實驗完畢后預從PdCl2溶液中分離出固體并稱量質量的實驗操作依次為:_______,_______,_______,稱量。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學用語是學習化學的重要工具,下列用來表示物質變化的化學用語中,正確的是
A. HCO3-在水溶液中的電離方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. Al3+的水解方程式:![]()
C. 鋼鐵發生電化學腐蝕的正極反應:Fe-2e-=Fe2+
D. 氫氧燃料電池的負極反應式:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
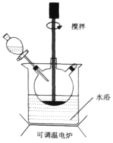
【題目】Fe(OH)3廣泛應用于醫藥制劑、顏料制造等領域,其制備步驟及裝置如下:在三頸燒瓶中加入16.7gFeSO4·7H2O和40.0ml蒸餾水。邊攪拌邊緩慢加入3.0mL濃H2SO4,再加入2.0gNaClO3固體。水浴加熱至80℃,攪拌一段時間后,加入NaOH溶液,充分反應。經過濾、洗滌、干燥得產品。
(1)NaClO3氧化FeSO4·7H2O的離子方程式為_____________。
(2)加入濃硫酸的作用為_________(填標號)。
a.提供酸性環境,增強NaClO3氧化性 b.脫去FeSO4·7H2O的結晶水
c.抑制Fe3+水解 d.作為氧化劑
(3)檢驗Fe2+已經完全被氧化需使用的試劑是_________。
(4)研究相同時間內溫度與NaClO3用量對Fe2+氧化效果的影響,設計對比實驗如下表
編號 | T/℃ | FeSO4·7H2O/g | NaClO3/g | 氧化效果/% |
i | 70 | 25 | 1.6 | a |
ii | 70 | 25 | m | b |
iii | 80 | n | 2.0 | c |
iv | 80 | 25 | 1.6 | 87.8 |
①m=______;n=______。
②若c>87.8>a,則a、b、c的大小關系為___________。
(5)加入NaOH溶液制備Fe(OH)3的過程中,若降低水浴溫度,Fe(OH)3的產率下降,其原因是___
(6)判斷Fe(OH)3沉淀洗滌干凈的實驗操作為_________________;
(7)設計實驗證明制得的產品含FeOOH(假設不含其他雜質)。___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)有甲、乙兩位同學均想利用原電池反應檢測金屬的活動性順序,兩人均用鎂片和鋁片作電極,但甲同學將電極放入1 mol·L-1的H2SO4溶液中,乙同學將電極放入1mol·L-1的NaOH溶液中,如圖所示。

①寫出甲中負極的電極反應式:__________。
②乙中負極反應式為__________,總反應的離子方程式:_______。
(2)將用導線相連的兩個鉑電極插入KOH溶液中,然后向兩極分別通入CH3OH(甲醇)和O2 ,則發生了原電池反應,該原電池中的負極反應式為________________;正極反應式為______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丙烯是一種重要的化工原料,可通過丁烯催化裂解或丁烯與甲醇耦合制備。
Ⅰ.丁烯催化裂解生產丙烯的反應方程式是2C4H8(g)![]() 2C3H6(g)+ C2H4(g)。
2C3H6(g)+ C2H4(g)。
(1)已知C4H8、C3H6、C2H4的燃燒熱分別為2710.0 kJ![]() mol-1、2050.0 kJ
mol-1、2050.0 kJ![]() mol-1、1410.0 kJ
mol-1、1410.0 kJ![]() mol-1,則該反應的ΔH=_______ kJ
mol-1,則該反應的ΔH=_______ kJ![]() mol-1。下列操作既能提高C4H8的平衡轉化率,又能加快反應速率的是_________。
mol-1。下列操作既能提高C4H8的平衡轉化率,又能加快反應速率的是_________。
A.升高溫度 B.增大壓強
C.增大C4H8的濃度 D.使用更高效的催化劑
(2)某溫度下,在體積為2 L的剛性密閉容器中充入2.00 mol C4H8進行上述反應,容器內的總壓強p隨時間t的變化如下表所示:
反應時間t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
總壓強p/kPa | 4.00 | 4.51 | 4.80 | 4.91 | 4.96 | 5.00 | 5.00 |
則0~10 min內υ(C4H8)=_______ mol![]() L-1
L-1![]() min-1,該溫度下的平衡常數K=_______kPa(用氣體的分壓表示)。
min-1,該溫度下的平衡常數K=_______kPa(用氣體的分壓表示)。
Ⅱ.將甲醇轉化耦合到丁烯裂解過程中生產丙烯,主要涉及下列反應:
① 2C4H8(g)![]() 2C3H6(g)+ 2H4(g) ΔH>0
2C3H6(g)+ 2H4(g) ΔH>0
② 2CH3OH(g)![]() C2H4(g) + 2H2O(g) ΔH<0
C2H4(g) + 2H2O(g) ΔH<0
③ C2H4(g)+ C4H8(g)![]() 2C3H6(g) ΔH<0
2C3H6(g) ΔH<0
已知:甲醇吸附在催化劑上,可以活化催化劑;甲醇濃度過大也會抑制丁烯在催化劑上的轉化。
(3)圖1是C3H6及某些副產物的產率與n(CH3OH)/n(C4H8)的關系曲線。最佳的n(CH3OH)/n(C4H8)約為_________。

(4)圖2是某壓強下,將CH3OH和C4H8按一定的物質的量之比投料,反應達到平衡時C3H6的體積分數隨溫度的變化曲線。由圖可知平衡時C3H6的體積分數隨溫度的升高呈現先升高后降低,其原因可能是__________________________________________________。

(5)下列有關將甲醇轉化耦合到丁烯裂解過程中生產丙烯的說法正確的是________。
A.增大甲醇的通入量一定可以促進丁烯裂解
B.甲醇轉化生成的水可以減少催化劑上的積碳,延長催化劑的壽命
C.提高甲醇與丁烯的物質的量的比值不能提高丙烯的平衡組成
D.將甲醇轉化引入丁烯的裂解中,可以實現反應熱效應平衡,降低能耗
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)標準狀況下,0.2mol NH3與_________________g H2O的電子數相等。
(2)含有相同氧原子數的CO和CO2,其質量比為_________________________。
(3)已知14g A和40g B恰好完全反應生成0.25mol C和38g D,則C的摩爾質量__________。
(4)已知V mLAl2(SO4)3溶液中含Al3+ a g,則溶液中SO42-的物質的量濃度是_____________。
(5)下列8種化學符號:11H2、12H2、614C、36Li、1123Na、714N、37Li、1224Mg。
①表示核素的符號共________種。
②互為同位素的是________。
③中子數相等,但質子數不相等的核素是_______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com