
【題目】利用天然氣熱裂解制取乙炔和氫氣近年來成為各國研究的熱點,發生的主要反應為:2CH4(g)![]() C2H2(g)+3H2(g) △H=a kJmol-1,副反應:2CH4(g)
C2H2(g)+3H2(g) △H=a kJmol-1,副反應:2CH4(g)![]() C2H4(g)+2H2(g) 回答下列問題:
C2H4(g)+2H2(g) 回答下列問題:
(1)天然氣熱裂解過程使用的催化劑中含有SiO2、Al2O3等多種難被還原的氧化物,寫出SiO2的另外兩種用途:_______________________,寫出Al2O3與苛性鉀溶液反應的離子方程式___________________;
(2)已知甲烷的燃燒熱△H=-890.3kJmol-1,乙炔的燃燒熱△H=-1299.6kJmol-1,氫氣的燃燒熱△H=-285.8kJmol-1,則上式中的a=___________;
(3)天然氣經重整催化作用生成氫氣,氫氣在下圖所示的燃料電池中放電(以熔融Li2CO3和K2CO3為電解質),寫出燃料極上發生的電極反應式_______________________________;

(4)某溫度下,向1L恒容密閉容器中充入0.3mol甲烷,控制條件使其只發生上述副反應,達到平衡時,測得c(C2H4)=c(CH4),則該條件下甲烷的平衡轉化率為__________;
(5)天然氣裂解過程中,平衡時各氣體分壓(單位為Pa)的對數(δ)與溫度(T)之間的關系如下圖:

①副反應2CH4(g)![]() C2H4(g)+2H2(g) 的△H__________(填“>”或“<”)0;
C2H4(g)+2H2(g) 的△H__________(填“>”或“<”)0;
②利用圖中數據計算A點溫度下主要反應2CH4(g)![]() C2H2(g)+3H2(g)的平衡常數__________(利用平衡分壓代替平衡濃度計算,
C2H2(g)+3H2(g)的平衡常數__________(利用平衡分壓代替平衡濃度計算,![]() )。
)。
【答案】(1)制玻璃、光纖(合理即可 ) Al2O3+2OH- =2AlO2- +H2O (2)+376.4
(3)H2 -2e-+ CO32- =H2O+CO2 (4)66.7% (5)① > ② 5×104Pa2
【解析】
試題分析:(1)SiO2可用來制玻璃及光學纖維等,Al2O3是兩性氧化物,能溶解于KOH,發生反應的離子方程式為Al2O3+2OH- =2AlO2- +H2O;
(2)已知:①CH4(g)+2O2 (g)═CO2(g)+2H2O(l)△H=-890.3kJmol-1 ;
②C2H2(g)+2.5O2(g)=2CO2 (g)+H2O(l)△H2=-1299.6kJ/mol;
③2H2 (g)+O2(g)=2H2O(l)△H3=-571.6kJ/mol;
將①×4-②-③×可得:
2CH4(g)=C2H2(g)+3H2 (g)△H=(-890.3kJmol-1 )×4-(-1299.6kJmol-1)-(-571.6kJmol-1)×=+376.4kJ/mol;
(3)通入甲烷的一極為原電池的負極,發生氧化反應,根據圖示信息知道負極電極反應式為:H2-2e-+CO32-=CO2+H2O;
(4)設CH4的轉化濃度為Xmol/L,可知:
2CH4(g)=C2H4(g)+2H2(g)
初始濃度:0.3mol/L 0 0
濃度變化:Xmol/L ![]() Xmol/L
Xmol/L
平衡濃度:(0.3-X)mol/L ![]() Xmol/L
Xmol/L
根據c(C2H4)=c(CH4)可知:0.3-X=![]()
解得X=0.2mol/L;
故CH4的平衡轉化率=![]() ×100%=66.7%;
×100%=66.7%;
(5)①反應2CH4(g)=C2H4(g)+2H2(g)為分解反應,而分解反應絕大多數為吸熱反應,故此反應為吸熱反應;
②結合圖像,根據此反應的平衡常數表達式,將氣體的平衡濃度換為平衡分壓,即K=![]() =
=![]() =5×104。
=5×104。


 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:
【題目】綠色化學對化學反應提出了“原子經濟性”(原子節約)的新概念及要求。理想的“原子經濟性”反應是原料分子中的原子全部轉變成所需產物,不產生副產物,實現零排放。以下反應中符合綠色化學原理的是
A.乙烯與氧氣在銀催化作用下生成環氧乙烷(![]() )
)
B.乙烷與氯氣制備氯乙烷
C.苯和乙醇為原料,在一定條件下生產乙苯
D.乙醇與濃硫酸共熱制備乙烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氣體分子中的極性鍵在紅外線的照射下,易像彈簧一樣做伸縮和彎曲運動,從而產生熱量而造成溫室效應。下列不屬于造成溫室效應氣體的是( )
A.CO2 B.N2O C.CH4 D.N2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】雷雨天閃電時空氣中有臭氧生成,下列說法正確的是( )
A.O2和O3互為同位素
B.O2和O3的相互轉化是物理變化
C.等物質的量的O2和O3含有相同的質子數
D.在相同的溫度與壓強下,等體積的O2和O3含有相同的分子數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于濃硝酸的敘述正確的是( )
A.具有揮發性,因而濃硝酸略帶有黃色
B.具有不穩定性,實驗室里應保存在棕色瓶中
C.具有氧化性,常溫下可以跟銅緩慢反應
D.具有酸性,實驗室可以用它來制氫氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種重要的有機化工原料有機物X,下面是以它為初始原料設計出如下轉化關系圖(部分產物、合成路線、反應條件略去)。Y是一種功能高分子材料。

已知:(1)X為芳香烴,其相對分子質量為92
(2)烷基苯在高錳酸鉀的作用下,側鏈被氧化成羧基:![]()
(3)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
請根據本題所給信息與所學知識回答下列問題:
(1)X的分子式為______________。
(2) 中官能團的名稱為____________________;
中官能團的名稱為____________________;
(3)反應③的反應類型是___________;已知A為一氯代物,則E的結構簡式是____________;
(4)反應④的化學方程式為_______________________;
(5)阿司匹林有多種同分異構體,滿足下列條件的同分異構體有________種:①含有苯環;②既不能發生水解反應,也不能發生銀鏡反應;③1mol該有機物能與2molNaHCO3完全反應。
(6)請寫出以A為原料制備![]() 的合成路線流程圖 (無機試劑任用)。合成路線流程圖示例如下:
的合成路線流程圖 (無機試劑任用)。合成路線流程圖示例如下:
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】 不能說明氧的非金屬性比硫強的事實是( )
A. H2O的熱穩定性強于H2S
B. 硫化氫水溶液露置于空氣中變渾濁
C. H2O是液體,H2S常溫下是氣體
D. 氧氣和氫氣化合比硫和氫氣化合容易
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(12分) 東晉《華陽國志南中志》卷四中已有關于白銅的記載,云南鎳白銅(銅鎳合金)聞名中外,曾主要用于造幣,亦可用于制作仿銀飾品。回答下列問題:
(1)鎳元素基態原子的電子排布式為_________,3d能級上的未成對的電子數為______。
(2)硫酸鎳溶于氨水形成[Ni(NH3)6]SO4藍色溶液。
①[Ni(NH3)6]SO4中陰離子的立體構型是_____。
②在[Ni(NH3)6]2+中Ni2+與NH3之間形成的化學鍵稱為_ _,提供孤電子對的成鍵原子是__ ___。
③氨的沸點_____(“高于”或“低于”)膦(PH3),原因是____ ;氨是____ _分子(填“極性”或“非極性”),中心原子的軌道雜化類型為____。
(3)單質銅及鎳都是由______鍵形成的晶體:元素同與鎳的第二電離能分別為:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是______。
(4)某鎳白銅合金的立方晶胞結構如圖所示。
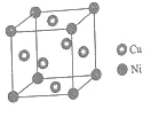
晶胞中銅原子與鎳原子的數量比為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組的學生從網上查得如下信息:①鈉能在CO2中燃燒。②常溫下CO能與PdCl2溶液反應得到黑色的Pd。經過分析討論,他們認為鈉在CO2中燃燒時,還原產物可能是碳、也可能是CO,氧化產物可能是Na2CO3。為驗證上述推斷,他們設計如下方案進行實驗,請回答下列問題。
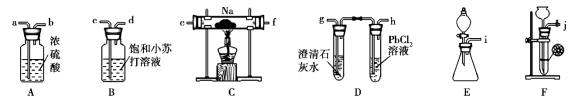
(1)他們欲用上述儀器組裝一套裝置:用石灰石與鹽酸反應制取CO2(能隨意控制反應的進行)來證明鈉能在CO2中燃燒并檢驗氣態還原產物,所用儀器接口連接順序為 ,制取CO2反應的離子方程式為 。
(2)裝置連接好后,首先要進行的實驗操作是 ,點燃酒精燈前,應進行的操作是 ,等裝置 (填寫裝置字母代號及現象)時,再點燃酒精燈,這步操作的目的是 。
(3)若裝置D的PdCl2溶液中有黑色沉淀,C中有殘留固體(只有一種物質),則C中反應的化學方程式為 ;若裝置D的PdCl2溶液中無黑色沉淀,C中有殘留固體(有兩種物質),則C中反應的化學方程式為 。
(4)后來有一位同學提出,鈉的氧化產物也可能是Na2O,因此要最終確定鈉的氧化產物是何種物質,還需要檢驗C中殘留的固體是否含有Na2O,為此,他認為應較長時間通入CO2以確保鈉反應完,然后按照如下方案進行實驗,可確定殘留固體中是否含有Na2O,他的實驗方案是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com