
【題目】我國化工專家侯德榜的“侯氏制堿法”曾為世界制堿工業做出了突出貢獻。他利用NaHCO3、NaCl、NH4C1等物質溶解度的差異,以食鹽、氨氣、二氧化碳等為原料制得NaHCO3,進而生產出純堿。以下A、B、 C、 D四個裝置可組裝成實驗室模擬“侯氏制堿法”制取NaHCO3的實驗裝置。裝置中分別盛有以下試劑:B:稀硫酸;C:鹽酸、碳酸鈣;D:含氨的飽和食鹽水、水。

四種鹽在不同溫度下的溶解度(g/100 g水)表(說明:①>35 ℃ NH4HCO3會有分解)

請回答以下問題:
(1)裝置的連接順序應是__________(填字母)。
(2)A裝置中盛放的試劑是__________,其作用是___________________。
(3)在實驗過程中,需要控制D溫度在30℃~35℃,原因是_________________。
(4)反應結束后,將錐形瓶浸在冷水中,析出NaHCO3晶體。用蒸餾水洗滌NaHCO3晶體的目的是除去____(雜質以化學式表示)。
(5)將錐形瓶中的產物過濾后,所得的母液中含有___________(以化學式表示),加入氯化氫,并進行_________操作,使NaCl溶液循環使用,同時可回收NH4Cl。
【答案】CADB 飽和NaHCO3溶液 除去CO2中的HCl 溫度超過35℃,碳酸氫銨開始分解,溫度太低,反應速率降低,不利于反應進行 NaCl、NH4C1、NH4HCO3 NaHCO3、NaCl、NH4C1、NH4HCO3 結晶
【解析】
侯氏制堿法,也稱為聯合制堿法,化學反應原理是用氨氣和二氧化碳與氯化鈉飽和溶液反應生成碳酸氫鈉,然后加熱碳酸氫鈉制取碳酸鈉,總化學反應方程式為NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,C裝置為反應發生裝置,裝有鹽酸、碳酸鈣,制取CO2氣體,B裝置為尾氣處理裝置,裝有稀硫酸,吸收反應中過量的NH3,D中裝有含氨的飽和食鹽水,反應要制取NaHCO3,需要除去反應產生的HCl氣體,則可判斷A裝置中應裝的是飽和NaHCO3溶液,目的是除去HCl氣體,據此分析解答。
(1)C裝置為反應發生裝置,B裝置為尾氣處理裝置,裝有稀硫酸,吸收反應中過量的NH3,D中裝有含氨的飽和食鹽水,反應要制取NaHCO3,則可判斷A裝置中應裝的是飽和NaHCO3溶液,因此裝置連接順序為CADB;
(2)利用NaHCO3的溶解度較小,可以析出晶體,可判斷A中裝的是NaHCO3飽和溶液,作用是除去CO2中的HCl;
(3)D為制取NaHCO3晶體,根據溶解度數據,反應應是先產生NH4HCO3,然后由于NaHCO3的溶解度比NH4HCO3小,對其進行降溫處理,繼而析出NaHCO3晶體,而要控制溫度在30℃~35℃,是由于碳酸氫銨易受熱分解,而溫度太低,化學反應速率太慢,不利于反應進行;
(4)反應結束后,將錐形瓶浸在冷水中,析出NaHCO3晶體。根據溶液中含有的物質可知用蒸餾水洗滌NaHCO3晶體的目的是除去NaCl、NH4C1、NH4HCO3雜質;
(5)將錐形瓶中的產物過濾后,所得的母液中含有NaHCO3、NaCl、NH4C1、NH4HCO3,加入氯化氫,還可以產生NaCl,而NaCl又是反應的原料,達到循環利用的目的,需進行結晶操作。


科目:高中化學 來源: 題型:
【題目】下列關于下圖所示電化學裝置的分析正確的是

A. 若X為直流電源,Y為銅棒接正極,則Fe棒上鍍銅
B. 若X為直流電源,Y為碳棒接負極,則Fe棒被保護
C. 若X為電流計,Y為鋅棒,則SO42-移向Fe棒
D. 若X為導線,Y為銅棒,則Fe棒發生還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學利用氧化還原反應:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4 +8H2O設計如下原電池,鹽橋中裝有飽和KCl溶液。下列說法正確的是

A. b電極上發生還原反應
B. 外電路電子的流向是從a到b
C. 電池工作時,鹽橋中的SO42-移向甲燒杯
D. a電極上發生的反應為:MnO4-+8H++5e- = Mn2++4H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對常溫下0.1mol/L的醋酸溶液,以下說法正確的是
A. 由水電離出來的c(H+)=1.0×10-13mol/L
B. c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-)
C. 與同濃度的鹽酸分別加水稀釋10倍:pH(醋酸) <pH(鹽酸)
D. 與等濃度等體積NaOH溶液反應后的溶液中:c(CH3COOH)+c(CH3COO-)=0.1mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外小組所做實驗的示意圖如圖所示:圖中“→”表示氣體流向, M是一種純凈而干燥的氣體,Y為另一種氣體,E內有紅棕色氣體產生,實驗所用物質只能由下列物質中選取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、堿石灰等固體及蒸餾水。據此實驗,完成下列填空:

(1)A中所用裝置的主要儀器和藥品是______________________。
(2)B中所選的干燥劑是________,其作用是______________________________。
(3)C中發生的主要反應的化學方程式:________________________________。
(4)制取Y氣體的D裝置所用的主要儀器是__________________________。
制取Y氣體的化學方程式是________________________。
(5)F中發生反應的化學方程式為__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25 ℃時,將濃度均為0.1 mol·L-1,體積分別為Va和Vb的HA溶液與BOH溶液按不同體積比混合,保持Va + Vb=100 mL,Va、Vb與混合液pH的關系如圖所示,下列說法正確的是
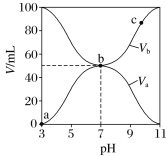
A. Ka(HA)=1×10-6
B. b點c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c過程中水的電離程度始終增大
D. c點時,![]() 隨溫度升高而減小
隨溫度升高而減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na、Al、Fe、Cu是中學化學中重要的元素,它們的單質及其化合物之間有很多轉化關系,如通常所說的“鐵三角”、“鋁三角”等。下表所列物質不能按如圖(“→”表示一步完成)關系相互轉化的是

A | B | C | D | |
a | NaHCO3 | Al | Fe | Cu(OH)2 |
b | NaOH | Al2O3 | FeCl3 | CuSO4 |
c | Na2CO3 | NaAlO2 | FeCl2 | CuCl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干種離子組成,取適量該溶液進行如下實驗:下列說法正確的是( )

A. 原溶液中一定只存在AlO2-、CO32-、SO42-、Cl- 四種離子
B. 氣體A的化學式是CO2,其電子式為O::C::O
C. 原溶液中一定不存在的離子是Cu2+、Ba2+、Fe3+
D. 生成沉淀B的離子方程式為:Al3++ 3OH- = Al(OH)3 ↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,有a.鹽酸 b.硫酸 c.醋酸三種酸:
(1)若三者c(H+)相同時,物質的量濃度由大到小的順序是____________。
(2)同體積、同物質的量濃度的三種酸,中和NaOH的能力由大到小的順序是______________。
(3)當三種酸物質的量濃度相同時,c(H+)由大到小的順序是__________。
(4)當三者c(H+)相同且體積也相同時,分別放入足量的鋅,相同狀況下產生氣體的體積由大到小的順序是__________________。
(5)將c(H+)相同的三種酸均加水稀釋至原來的100倍后,c(H+)由大到小的順序是____________。
(6)當c(H+)相同、體積相同時,同時加入形狀、密度、質量完全相同的鋅,若產生相同體積的H2(相同狀況),則開始時反應速率的大小關系為_______。反應所需時間的長短關系是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com