
【題目】常溫下,有體積相同的四種溶液:![]() 的
的![]() 溶液;
溶液;![]() 的硫酸;
的硫酸;![]() 的氨水;
的氨水;![]() 的NaOH溶液.下列說法正確的是
的NaOH溶液.下列說法正確的是![]()
A.![]() 和
和![]() 混合后
混合后![]()
B.![]() 和
和![]() 溶液中:
溶液中:![]()
C.![]() 和
和![]() 混合溶液中:
混合溶液中:![]()
D.四種溶液各稀釋100倍,溶液pH:![]()
 同步練習河南大學出版社系列答案
同步練習河南大學出版社系列答案科目:高中化學 來源: 題型:
【題目】實驗研究發現,硝酸發生氧化還原反應時,硝酸的濃度越稀,對應還原產物中氮元素的化合價越低。現有一定量的鋁粉和鐵粉的混合物與一定量很稀的硝酸充分反應,反應過程中無氣體放出。在反應結束后的溶液中逐滴加入![]() 溶液,所加NaOH溶液的體積
溶液,所加NaOH溶液的體積![]() 與產生沉淀的物質的量
與產生沉淀的物質的量![]() 關系如下圖所示,下列說法不正確的是
關系如下圖所示,下列說法不正確的是 ![]()
![]()
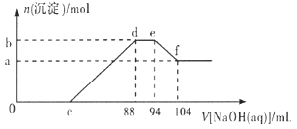
A.稀硝酸與鋁粉、鐵粉反應,其還原產物為硝酸銨
B.c點對應溶液的體積為![]()
C.b點與a點的差值為![]()
D.樣品中鋁粉和鐵粉的物質的量之比為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把質量為mg的銅絲灼燒變黑,立即放入下列物質中,能使銅絲變紅而且質量仍為mg的是
A.NaOH溶液B.CH3COOHC.稀HNO3D.CH3CH2OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】回答下列問題:
(1)某溫度時,測得0.01mol/L的NaOH溶液pH=13,該溫度下水的Kw=__。
(2)蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25.0kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-48.0kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
寫出CO氣體還原FeO固體得到Fe固體和CO2氣體的熱化學反應方程式:__。
(3)已知25℃時Ksp(Mg(OH)2)=1.8×10-11,為除去某食鹽溶液中的Mg2+,可用NaOH為除雜試劑,當控制溶液pH=12時,可確保Mg2+除盡,此時溶液中Mg2+的物質的量濃度為__mol/L。
(4)生活中明礬常作凈水劑,其凈水的原理是__(用離子方程式表示)。
(5)常溫下,取0.2mol/LHCl溶液與0.2mol/LMOH溶液等體積混合,測得混合溶液后的pH=5,寫出MOH的電離方程式:__。
(6)0.1mol/L的NaHA溶液中,已知有關粒子濃度由大到小的順序為:c(Na+)>c(HA-)>c(H2A)>c(A2-)
①該溶液中c(H+)__c(OH-)(填“>”、“<”或“=”)
②作出上述判斷的依據是__(用文字解釋)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色溶液X,由Na+、Mg2+、Ba2+、Al3+、AlO2-、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干種離子組成,取溶液進行如下連續實驗:
中的若干種離子組成,取溶液進行如下連續實驗:
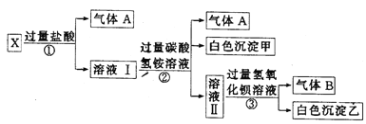
(1)氣體A的成分是_______(填電子式),氣體B的成分是_______(填結構式)
(2)X溶液中一定不存在的離子是______________。
(3)寫出步驟①中發生反應的所有離子方程式:________________。
(4)寫出步驟②中形成白色沉淀的離子方程式:________________。
(5)通過上述實驗,溶液X中不能確定是否存在的離子是______________;只要設計一個簡單的后續實驗就可以確定該離子是否存在,該方法是__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】繼電器在控制電路中應用非常廣泛,有一種新型繼電器是以對電池的循環充放電實現自動離合(如圖所示)。以下關于該繼電器的說法中錯誤的是
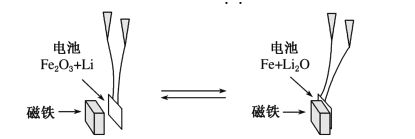
已知電極材料為納米Fe2O3,另一極為金屬鋰和石墨的復合材料。
A.充電完成時,電池能被磁鐵吸引
B.該電池電解液一般由高純度的有機溶劑、鋰鹽等原料組成
C.充電時,該電池正極的電極反應式為3Li2O+2Fe-6e-═Fe2O3+6Li+
D.放電時,Li作電池的負極,Fe2O3作電池的正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.1mol苯甲酸在濃H2SO4存在下與足量乙醇反應可得1mol苯甲酸乙酯
B.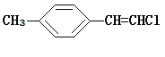 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
C.分子式為C5H12O的醇,能在銅催化下被O2氧化為醛的同分異構體有4種
D.1mol阿司匹林(結構簡式見圖)與足量的氫氧化鈉溶液加熱反應,最多消耗的氫氧化鈉的物質的量2mol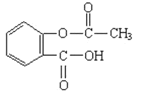
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】M為一種醫藥的中間體,其合成路線為:
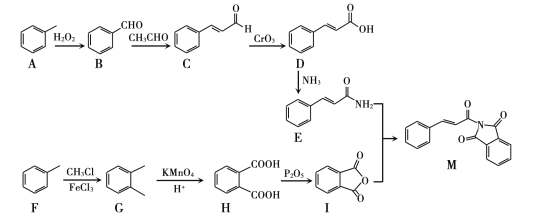
(1)A的名稱____。
(2)C中含有的含氧官能團名稱是____。
(3)F生成G的反應類型為____。
(4)寫出符合下列條件的D的同分異構體的結構簡式____
①能發生銀鏡反應 ②遇到FeCl3溶液顯紫色 ③苯環上一氯代物只有兩種
(5)H與乙二醇可生成聚酯,請寫出其反應方程式____
(6)寫出化合物I與尿素(H2N - CO - NH2)以2:1反應的化學方程式____
(7)參考題中信息,以1,3-丁二烯(CH2=CHCH= CH2)為原料,合成 ,寫出合成路線流程圖(無機試劑任選)____。
,寫出合成路線流程圖(無機試劑任選)____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一種新化合物(如圖所示),其中W、X、Y、Z 為同一短周期元素,Z 核外最外層電子數比X 核外電子數多1。下列敘述正確的是( )
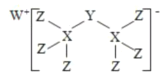
A.WZ 的熔點低于XZ4
B.元素非金屬性的順序為![]()
C.該新化合物中Y 不滿足8 電子穩定結構
D.Y 的最高價氧化物的水化物是強酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com