
【題目】把濃硫酸滴入濃鹽酸中會有氯化氫氣體逸出,對此現象的合理解釋是( )
A.氯化氫難溶于水
B.濃硫酸是一種高沸點的酸
C.濃硫酸有脫水性
D.濃硫酸溶于水放出大量的熱,降低了氯化氫的溶解度
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】CuBr是一種白色晶體,見光或潮濕時受熱易分解,在空氣中逐漸變為淺綠色。實驗室制備CuBr的反應原理為:SO2+2CuSO4+2NaBr+ 2H2O=2CuBr↓+2H2SO4+Na2SO4,用下列裝置進行實驗,不能達到實驗目的的是
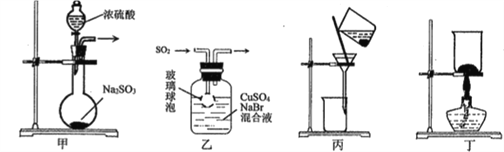
A. 用裝置甲制取SO2 B. 用裝置乙制取CuBr
C. 用裝置丙避光將CuBr與母液分離 D. 用裝置丁干燥CuBr
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.氮的固定一直是科學家研究的重要課題,合成氨則是人工固氮比較成熟的技術,其原理為N2 (g)+3H2 (g)![]() 2NH3(g)
2NH3(g)
(1)已知每破壞1mol有關化學鍵需要的能量如下表:
H-H | N-H | N-N | N≡N |
435.9kJ | 390.8kJ | 192.8kJ | 945.8kJ |
(1)則反應物的總能量_________(填“>”或 “<”)生成物的總能量
(2)在一定溫度下、向2L密閉容器中加入2 molN2、6 mol H2,在適當的催化劑作用下,發生反應 N2 (g)+3H2 (g)![]() 2NH3(g),10min后達到平衡,此時剩余4.5mol H2。
2NH3(g),10min后達到平衡,此時剩余4.5mol H2。
①下列敘述能說明此反應達到平衡狀態的是____。
a.容器內總壓強不變 b.v(H2)正=v(H2)逆 c.N2和H2的濃度相等
d. 2 mol NH3生成的同時有3 moH—H鍵斷裂 e.NH3的濃度不再改變
②0~10 min內的平均反應速率v(H2) 是____mol/(Lmin);10秒末NH3的濃度是___mol/L;N2 的的物質的量___mol
Ⅱ.某溫度時,在一個2L的密閉容器中X、Y、Z三種氣體物質的物質的量隨時間的變化曲線如圖所示,據此回答:
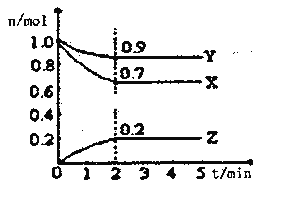
(1)該反應的化學方程式為___________
(2)從開始至2min,Z的平均反應速率為____________;
(3)改變下列條件,可以加快化學反應速率的有_________
A.升高溫度 B.減小物質X的物質的量 C.減小壓強 D.增加物質Z的物質的量. E.加入某種催化劑 F.縮小容積 G.使用效率更高的催化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向恒溫恒容的密閉容器中充入H2(g)和I2(g)各0.1mol,發生反應H2(g)+I2(g)![]() 2HI(g),該反應的能量變化如圖所示。下列說法正確的是( )
2HI(g),該反應的能量變化如圖所示。下列說法正確的是( )
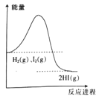
A. 該反應是吸熱反應
B. 斷裂0.05molH-H鍵和0.05molI-I鍵消耗的總能量小于生成0.1molH-I鍵釋放的總能量
C. 當容器中氣體密度不變時,說明反應已達到平衡狀態
D. 達到平衡時,生成HI的分子數約為0.2×6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醇與氫鹵酸反應是制備鹵代烴的重要方法。實驗室制備溴乙烷和1—溴丁烷的反應如下:
NaBr+H2SO4HBr+NaHSO4 ①
R—OH+HBr![]() R—Br+H2O ②
R—Br+H2O ②
可能存在的副反應有:醇在濃硫酸的存在下脫水生成烯和醚,Br—被濃硫酸氧化為Br2等。有關數據列表如下;
乙醇 | 溴乙烷 | 正丁醇 | 1—溴丁烷 | |
密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
沸點/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
請回答下列問題:
(1)溴乙烷和1—溴丁烷的制備實驗中,下列儀器最不可能用到的是________。(填字母)
a.圓底燒瓶 b.量筒 c.錐形瓶 d.長頸漏斗
(2)溴代烴的水溶性______(填“大于”、“等于”或“小于”)相應的醇,將1-溴丁烷粗產品置于分液漏斗中加水,振蕩后靜置,產物在______(填“上層”、“下層”或“不分層”)
(3)制備操作中,加入的濃硫酸必需進行稀釋,其目的是____________。(填字母)
a.減少副產物烯和醚的生成 b.減少Br2的生成
c.減少HBr的揮發 d.水是反應的催化劑
(4)欲除去溴代烷中的少量雜質Br2,下列物質中最適合的是____________。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制備溴乙烷時,采用邊反應邊蒸出產物的方法,其有利于______________ ;
但在制備1—溴丁烷時卻不能邊反應邊蒸出產物,其原因是_______________________。
(6)得到的溴乙烷中含有少量乙醇,為了制得純凈的溴乙烷,可用蒸餾水洗滌,分液后,再加入無水CaCl2后進行的實驗操作是______(填字母)
a.分液 b.蒸餾 c.萃取 d.過濾
(7)為了檢驗溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后______(按實驗的操作順序選填下列序號)①加熱 ②加入AgNO3 ③加入稀HNO3 ④加入NaOH溶液.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學利用反應Cu+2FeCl3=CuCl2+2FeCl2,設計了如圖所示的原電池裝置,下列說法正確的是( )
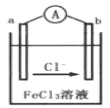
A. b為負極,發生還原反應
B. b電極反應式為2Fe3++2e-=Fe2+
C. 電子流動方向是a電極→FeCl3溶液→b電極
D. 電池的正極材料可以選用石墨、鉑電極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中,正確的是 ( )
A. 同溫同壓下,反應H2(g)+Cl2(g)=2HCl(g)在光照和點燃條件下的ΔH不同
B. 用銅作電極電解稀硫酸,反應Cu+H2SO4 ![]() CuSO4+H2↑可以發生
CuSO4+H2↑可以發生
C. 鉛蓄電池放電時的負極和充電時的陽極均發生還原反應
D. 使用催化劑,可加快反應速率,改變反應限度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A. 丙烷和丁烷互稱為同系物
B. ![]() 的名稱為3-甲基丁烷
的名稱為3-甲基丁烷
C. 沸點:正丁烷>異丁烷>丙烷
D. CH3CH2CH2CH3和CH3CH(CH3)2互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“封管實驗”具有簡易、方便、節約、綠色等優點,觀察下面四個“封管實驗”(夾持裝置未畫出),下列說法正確的是
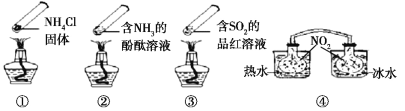
A. 加熱時,①封管上部匯集了固體NH4Cl,說明NH4Cl的熱穩定性比較好
B. 加熱時,②、③溶液均變紅,冷卻后又都變為無色
C. ④中,浸泡在熱水中的容器內氣體顏色變深,浸泡在冰水中的容器內氣體顏色變淺
D. 四個“封管實驗”中所發生的化學反應都是可逆反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com