
【題目】下列各組物質中,含原子數最多的是( )
A.標準狀況下5.6L 氫氣 B.4℃時9mL水
C.11gCO2 D.6.02×1022個H2SO4
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】合成氨反應為 N2(g)+3H2(g) ![]() 2NH3(g)△H=+92.4kJmol﹣1,下列說法正確的是( )
2NH3(g)△H=+92.4kJmol﹣1,下列說法正確的是( )
A.一定條件下,當N2的生成速率與N2的分解速率相等時,該反應處于平衡狀態
B.取1mol N2和3mol H2放在密閉容器內反應達平衡時,生成2 mol NH3
C.一定條件下反應達到平衡,再充入N2,則正反應速率增大,逆反應速率減小
D.一定條件下反應達到平衡,若升高溫度,反應速率增大,平衡向正反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中和熱的測定是重要的定量實驗。取0.55mol/L的NaOH溶液50mL與0.50mol/L的鹽酸50mL置于下圖所示的裝置中進行中和熱的測定實驗,回答下列問題:
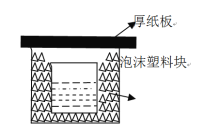
(1)從圖中實驗裝置看,其中尚缺少的兩種玻璃用品是_,為保證該實驗成功,該同學采取了許多措施,如圖的泡沫塑料塊的作用在于。
(2)倒入NaOH溶液的正確操作是:(從下列選出)。
A.沿玻璃棒緩慢倒入
B.分三次少量倒入
C.一次迅速倒入
D.簡述測量溫度的方法
(3)實驗記錄數據如表
項目 | 反應起始溫度T1(℃) | 終止溫度T2(℃) | T2-T1 | ||
HCl | NaOH | 平均溫度 | |||
第1次 | 26.2 | 26.0 | 29.4 | ||
第2次 | 27.0 | 27.4 | 32.2 | ||
第3次 | 25.9 | 25.9 | 29.1 | ||
第4次 | 26.4 | 26.2 | 29.7 | ||
設0.55mol/LNaOH溶液和0.50mol/L鹽酸溶液的密度都是1g/cm3,中和后生成溶液的比熱容c=4.18J/(g·℃)。則中和熱ΔH=(取到小數點后一位)。
(4)不能用醋酸代替鹽酸做此實驗,原因是____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在不同溫度下,水溶液中c(H+)與c(OH-)關系如圖所示。下列說法不正確的是
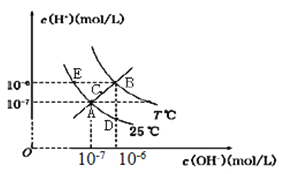
A.圖中五點Kw間的關系:B>C>A=D=E
B.E點對應的水溶液中,可能有NH4+、Ba2+、Cl-、I-大量同時存在
C.若0.1 mol/L 的NaHA 溶液水溶液中c(H+)與c(OH-)關系如圖D 點所示,則溶液中有: c(HA-)>c(OH-)>c(A2-)>c(H2A)
D.向NaHSO4溶液中滴入Ba(OH)2溶液,當c(H+)與c(OH-)關系如圖A點所示,則溶液中反應:2H+ + SO42- + Ba2+ + 2OH- = BaSO4↓+ 2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.高錳酸鉀是錳的重要化合物和常用氧化劑,在實驗室和醫療上有非常廣泛的應用。如圖1是工業上用軟錳礦(主要含MnO2)制備高錳酸鉀晶體的一種工藝流程:

(1)第①步加熱熔融應在鐵坩堝中進行,而不用瓷坩堝的原因是(用化學方程式表示)。寫出反應①的離子方程式;
(2)反應②的產物中,氧化產物與還原產物的物質的量的比是
(3)反應②中“酸化”時應選擇下列酸中的(填序號)
a.稀鹽酸b.稀硫酸c.亞硫酸
(4)操作Ⅱ的名稱是,實驗室進行該操作需用到的玻璃儀器有
Ⅱ.某小組設計如圖所示的裝置圖(圖中夾持和加熱裝置略去),分別研究SO2和Cl2的性質

(5)若從左端分別通入SO2和Cl2,裝置A中觀察到的現象是否相同?(填“相同”或“不相同”)。
(6)若裝置B中裝有5.0mL1.0mol/L的碘水,當通入足量Cl2完全反應后,共轉移了5.0×10-2mol電子,該反應的化學方程式為;
(7)若由元素S和O組成-2價酸根離子X,X中S和O的質量比為4∶3。當Cl2與含X的溶液完全反應后,有淺黃色沉淀產生,取少量上層清加入鹽酸酸化的氯化鋇溶液,有白色沉淀產生。寫出Cl2與含X的溶液反應的離子方程式。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com