
【題目】下列分子或離子中,不存在sp3雜化類型的是
A. SO42-B. NH3C. C2H6D. SO2
科目:高中化學 來源: 題型:
【題目】某陽離子Mn+的核外共有x個電子,核內有a個中子,則M的質量數為 ( )
A. a+x-n B. a-x+n
C. a-x-n D. .a+x+n
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.向Na2CO3溶液中逐滴加入HCl,直到不再生成CO2氣體為止,在此過程中.溶液中的HCO3-濃度變化是先變大后變小(溶液體積變化均忽略不計)
B.向NaHCO3溶液中加入Ba(OH)2固體,CO32-的濃度變化是先變大后變小(溶液體積變化均忽略不計)
C.有含0.2molNa2CO3和含0.3molHCl的兩種溶液:①將Na2CO3溶液逐滴滴入HCl溶液中;②將HCl溶液逐滴滴入Na2CO3溶液中,①②兩種操作生成的CO2體積之比為3:2
D.將等質量的Na2O和Na2O2樣品分別放入等量的水中,所得溶液的質量分數分別為a%和b%,則a、b的關系是a=b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ClO2是一種消毒、殺菌效率高、二次污染小的水處理劑。實驗室可通過以下反應制得:(已知H2C2O4中的碳為+3價)2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。試回答下列問題。
(1)該反應中氧化產物的化學式是___________;被還原的元素是___________。
(2)用雙線橋標出上述反應的電子轉移情況______。
2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
(3)若反應共產生了4.48L氣體(標準狀況),則反應轉移電子的物質的量為_________mol,消耗還原劑的物質的量為___________mol。
(4)標準狀況下44.8mL的ClO2氣體恰好能與50mL 0.1mol·L-1的Na2SO3溶液液完全反應,生成Na2SO4,氯元素在產物中的化合價為___________;此過程說明ClO2具有____(填“氧化”或“還原”)性。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向下列各溶液中通入足量CO2氣體,最終有渾濁現象產生的是
①飽和Na2CO3溶液 ②澄清石灰水 ③NaAlO2溶液
④CaCl2溶液 ⑤Na2SiO3溶液
A. 全部 B. 除①④⑤外
C. 除①②④外 D. 除②④外
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應中的能量變化是由化學反應中舊化學鍵斷裂時吸收的能量與新化學鍵形成時放出的能量不同引起的。如圖為N2(g)和O2(g)反應生成NO(g)過程中的能量變化,下列說法中正確的是( )
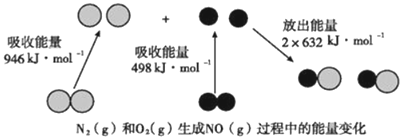
A. 1mol N2(g)和1mol O2(g)完全反應放出的能量為180kJ
B. 通常情況下,N2(g)和O2(g)混合能直接生成NO
C. 1mol N2(g)和1mol O2(g)具有的總能量小于2mol NO(g)具有的總能量
D. NO是一種酸性氧化物,能與NaOH溶液反應生成鹽和水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是某燃煤發電廠處理廢氣的裝置示意圖.下列說法正確的是( )

A. 此過程中沒有分解反應
B. 整個過程的反應可表示為: 2SO2+2CaCO3+O2═2CaSO4+2CO2
C. 使用此廢氣處理裝置可減少CO2的排放
D. 此過程中S元素的化合價未發生改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電解質溶液中粒子濃度關系正確的是( )
A. pH=1的NaHSO4溶液: c(H+)=c(SO![]() )+c(OH-)
)+c(OH-)
B. 含有AgCl和AgI固體的懸濁液: c(Ag+)>c(Cl-)=c(I-)
C. CO2的水溶液:c(H+)>c(HCO![]() )=2c(CO
)=2c(CO![]() )
)
D. 含等物質的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O![]() )+c(C2O
)+c(C2O![]() )+c(H2C2O4)]
)+c(H2C2O4)]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活生產密切相關,下列說法中正確的是( )
A. “青蒿一握,以水二升漬,絞取汁”,青蒿素的提取屬于化學變化
B. 光導纖維在信息領域應用越來越廣泛,其主要成分為SiO2
C. 燃煤中加入CaO可以減少酸雨的形成及溫室氣體的排放
D. 明礬凈水過程不涉及化學變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com