
���}Ŀ����֪�����cҺ�����廯�F�Ĵ������¿��l(f��)�Sɫ�����������屽��ijͬ�W����D���b����ȡ�屽���C���l(f��)������ȡ�������������Һ©���м��뱽��Һ�壬�ٌ����Һ�������뷴����A��A�¶˻����P�]���У���֪��������屽�С�
��1������A�з����Ļ��W����ʽ______________________________________________________
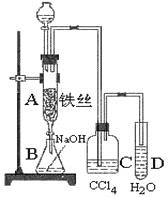
��2�����Y���r�����_A�¶˵Ļ���������Һ����B�У������ʎ��Ŀ����________________________________���������P�����Ļ��W����ʽ______________________________________��
��3�� C��ʢ��CCl4��������______________________________��
��4����ԇ��D�м���AgNO3��Һ�����a(ch��n)�����Sɫ�������t���C��ԓ������ȡ����������һ�N�C���ķ�����_______________��
���𰸡� ![]() ��ȥ�����屽�е��� Br2+2NaOH=NaBr+NaBrO+H2O ��ȥ�廯����w�е�������ͱ����� ��ԇ��D�м���ʯ��ԇҺ������Һ׃�tɫ���tԓ������ȡ������
��ȥ�����屽�е��� Br2+2NaOH=NaBr+NaBrO+H2O ��ȥ�廯����w�е�������ͱ����� ��ԇ��D�м���ʯ��ԇҺ������Һ׃�tɫ���tԓ������ȡ������
����������1���b��A���Á��Ƃ��屽�ģ�����A�з����Ļ��W����ʽ��![]() ����2���������ɵ��屽�к����ܽ�Ć��|�壬��������Һ����������c��Һ�е�Ŀ���dz�ȥ�����屽�е��壬���P�����ķ���ʽ��Br2��2NaOH��NaBr��NaBrO��H2O��3Br2��6NaOH��5NaBr��NaBrO3��3H2O����3�����ڱ��͆��|���ד]�l(f��)�����ɔ_�廯��ęz�������Ȼ�̼�������dz�ȥ�廯����w�е�������ͱ���������5�������廯������ˮ��Һ�@���ԣ���(j��)���OӋ�ęz���飺��ԇ��D�м���ʯ��ԇҺ������Һ׃�tɫ���tԓ������ȡ��������
����2���������ɵ��屽�к����ܽ�Ć��|�壬��������Һ����������c��Һ�е�Ŀ���dz�ȥ�����屽�е��壬���P�����ķ���ʽ��Br2��2NaOH��NaBr��NaBrO��H2O��3Br2��6NaOH��5NaBr��NaBrO3��3H2O����3�����ڱ��͆��|���ד]�l(f��)�����ɔ_�廯��ęz�������Ȼ�̼�������dz�ȥ�廯����w�е�������ͱ���������5�������廯������ˮ��Һ�@���ԣ���(j��)���OӋ�ęz���飺��ԇ��D�м���ʯ��ԇҺ������Һ׃�tɫ���tԓ������ȡ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� С�W��10��犑����}ϵ�д�
С�W��10��犑����}ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����V��W��X��Y��Z��NԪ�أ�������ԭ����(sh��)���������Ҷ�С��20;����X��Z�ǽ���Ԫ�ء���֪V��Z��ͬһ�壬����ԭ��������ӌ���ֻ��1�����,W��YҲ��ͬһ�壬Wԭ��������ӌ�����Ӕ�(sh��)�Ǵ�����ӌ�����Ӕ�(sh��)��3��,Xԭ��������ӌ�����Ӕ�(sh��)����Yԭ��������ӌ�����Ӕ�(sh��)��һ�롣Ո�����P��Ԫ�ط�̖�ش�
��1��X��Z���Ե���߃r���������ˮ������Է������}��ˮ��ԓ�������x�ӷ���ʽ��_____________��
��2��X��߃r���������ˮ������ˮ����x����ʽ�飺____________________________________��
��3��W�cZ ���γɻ�����Z2W2��ԓ����������ʽ�� ______________________________________��
��4��Y�cZ�γɵĻ�����ˮ��ҺpH ______ 7��������������������������x�ӷ���ʽ��ʾ��ԭ�� ____________________________________________________________��
��5���˜ʠ�r�£�Y����߃r�������oɫ���w��ԓ�l����0.20 molԓ���|�cһ����Һ�B(t��i)ˮ��ϵõ�һ�Nϡ��Һ�����ų�Q kJ�ğ���������ԓ�����ğữ�W����ʽ��________________________________��
��6��W�cV ���γɻ�����V2W2��ԓ������ĽY��ʽ�� ______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���������|��,���ܺ���ϩ�l(f��)���ӳɷ�������( )��
A. H2 B. H2O C. KMnO4 D. Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������f�������_����
A���ͷֽⷴ��һ����������߀ԭ����
B���ÓQ����һ��������߀ԭ����
C���І��|���ӵķ���һ��������߀ԭ����
D���І��|���ɵķֽⷴ��һ��������߀ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������P�ڝ�����͝�����Ĕ������_���ǣ�������
A.��������һ�N������܉���ﰱ�⡢���Ț��w
B.��������в���(w��n)���ԣ���������������ɫƿ��
C.�����£���������Ը��~������������������c�~ƬѸ�ٷ���
D.����ҿ����Ý�������ƚ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���F(xi��n)���ĽMҺ�w�����Ȼ��c��Һ�����Ȼ�̼�M�ɵĻ��Һ ���Ҵ�ˮ��Һ ���Ȼ��c�͆��|���ˮ��Һ ��̼���}���Ȼ��}��Һ�����x���ϸ����Һ�����_���������ǣ�������
A.��Һ����ȡ�����s�����l(f��)
B.��ȡ�����s����Һ���^�V
C.��Һ�����s����ȡ���^�V
D.���s����ȡ����Һ���^�V
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����ڱ���ǰ20̖�NԪ�أ������P��Ϣ���£��?sh��)�ԭ�Ӱ돽�?.089nm����Fԭ���Пo���ӣ�G�ڵؚ��к����ӵڶ�λ��HԪ����ɫ��������ɫ������(j��)�}��Ո�ش����І��}��
Ԫ�ش�̖ | A | B | C | D | E |
ԭ�Ӱ돽/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
��Ҫ���σr | +5����3 | +3 | +6����2 | ��1 | ��2 |
��1��B��ԭ�ӽY��ʾ��D��___________��
��2��F2C��F2E�ɷN�������У����c�^�ߵ���____����Wʽ����
��3�������ʽ��ʾ������H2E���γ��^��_______________________________��
��4��ijͬ�W�OӋ����Gͬ��Ķ�����Ԫ�ص���̓r�仯���ȼ�ϵ�늳أ�늽��|��KOH�� �tԓ늳ص�ؓ�O��늘O����ʽ��__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����֪������NaH+H2O=H2+NaOH����ԓ�������Д����_���ǣ�������
A.1mol NaH���ӷ���ʧȥ1mol���
B.ÿ����1mol H2�D��2mol���
C.NaH����������������߀ԭ��
D.NaOH�������a(ch��n)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������f���У������_���ǣ� ��
A.���ǿ����{ζ��
B.�F�ۿ�����������
C.̼����c��������ˎ
D.��ʯ�ҿ���ʳƷ���
�鿴�𰸺ͽ���>>
���H�WУ��(y��u)�x - �������б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com