
【題目】短周期中三種元素a、b、c在周期表中的位置如圖所示,下列有關這三種元素的說法正確的是
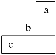
A. a是一種活潑的非金屬元素B. b的氣態氫化物比c的穩定
C. c的氧化物對應的水化物是強酸D. b元素的最高化合價為+7價
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】已知反應A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列說法正確的是( )
2AB2(g) ΔH<0,下列說法正確的是( )
A. 達到平衡后,升高溫度或增大壓強都有利于該反應平衡正向移動
B. 達到平衡后,降低溫度或減小壓強都有利于該反應平衡正向移動
C. 升高溫度有利于反應速率增加,從而縮短達到平衡的時間
D. 升高溫度,正向反應速率增加,逆向反應速率減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如圖所示裝置(夾持儀器省略)進行實驗,將液體A逐漸加入固體B中。回答下列問題:
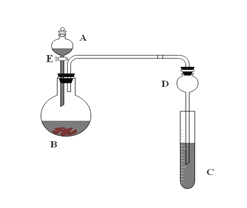
(1)圖中D裝置在實驗中的作用____________________;
(2)若A中為濃鹽酸,B中為高錳酸鉀,C中盛有KI淀粉溶液,旋開E后,C中的現象是溶液變藍色,試寫出A與B反應的化學方程式_________________________:
(3)若A為濃氨水,B為生石灰,C中盛有AlCl3溶液,旋開E足夠長的時間后,C中的現象是____________________,C中發生反應的化學方程式為:__________;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將5 mL 0.005 mol·L-1 FeCl3溶液和5 mL 0.015 mol·L-1 KSCN溶液混合。達到平衡后溶液呈紅色。再將混合液等分為5份,分別進行如下實驗:
| 實驗①:滴加4滴水,振蕩 |
實驗②:滴加4滴飽和FeCl3溶液,振蕩 | |
實驗③:滴加4滴1 mol·L-1 KCl溶液,振蕩 | |
實驗④:滴加4滴1 mol·L-1 KSCN溶液,振蕩 | |
實驗⑤:滴加4滴6 mol·L-1 NaOH溶液,振蕩 |
下列說法不正確的是
A. 對比實驗①和②,為了證明增加反應物濃度,平衡發生正向移動
B. 對比實驗①和③,為了證明增加生成物濃度,平衡發生逆向移動
C. 對比實驗①和④,為了證明增加反應物濃度,平衡發生正向移動
D. 對比實驗①和⑤,為了證明減少反應物濃度,平衡發生逆向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A.明礬、小蘇打、醋酸、次氯酸均為電解質
B.碘酒、牛奶、豆漿、漂白精均為膠體
C.根據是否具有丁達爾現象可將分散系分為溶液、膠體和濁液
D.物質可根據在水中或熔化狀態下的導電性分為電解質與非電解質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關鹵素的說法不正確的是
A. ICl在反應ICl+2NaOH![]() NaCl+NaIO+H2O中作氧化劑
NaCl+NaIO+H2O中作氧化劑
B. 金屬鈉與氯氣反應生成氯化鈉后,其結構的穩定性增強,體系的能量降低
C. 淀粉碘化鉀在空氣中變藍,發生了4I-+ O2 + 2H2O![]() 2I2 + 4OH-
2I2 + 4OH-
D. HF、HCl、HBr、HI的熱穩定性依次減弱,還原性依次增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組學習了亞鐵鹽的性質后,欲探究FeSO4溶液分別與Na2CO3溶液、NaHCO3溶液的反應。已知:Fe(OH)2和FeCO3均為白色沉淀,不存在Fe(HCO3)2。實驗操作及現象記錄如下:
實驗 | 試劑 | 操作及現象 | ||
試管(I) | 試管(II) | |||
(試管容積為50 mL) | 實驗a | 1.0 mol·L-1 FeSO4溶液 24 mL | 1.0 mol·L-1 Na2CO3溶液24mL | 傾倒完后,迅速用膠塞塞緊試管I的口部,反復上下顛倒搖勻,使反應物充分混合 反應過程中無氣泡產生,生成白色絮狀沉淀 放置1.5~2 h后,白色絮狀沉淀轉化為白色顆粒狀沉淀 |
實驗b | 1.0 mol·L-1 FeSO4溶液 10 mL | 1.0 mol·L-1 NaHCO3溶液 20 mL | 傾倒完后,迅速產生白色顆粒狀沉淀和大量氣泡。振蕩,經2~4 min后液面上方試管內壁粘附的白色顆粒狀沉淀物變成紅褐色 | |
(1)甲同學認為實驗a中白色顆粒狀沉淀是FeCO3,寫出該反應的離子方程式:________;他為了證實自己的觀點,進行實驗:取少量白色顆粒狀沉淀,加入________,發現產生大量氣泡。
(2)乙同學推測實驗a的白色顆粒狀沉淀中還可能含有Fe(OH)2,他將實驗a中兩種溶液體積均改成15 mL后再進行實驗,證實了他的推測。能證明Fe(OH)2存在的實驗現象是_________。
(3)實驗b中白色顆粒狀沉淀主要成分也為FeCO3,寫出生成FeCO3的離子方程式:________。
(4)實驗b中液面上方試管內壁粘附的白色顆粒狀沉淀物變成紅褐色,主要原因是潮濕的FeCO3被氧氣氧化,寫出該反應的化學方程式:__________。
(5)乙同學反思,實驗a中含有Fe(OH)2,實驗b中幾乎不含有Fe(OH)2,對比分析出現差異的原因是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表各組物質之間通過一步反應不可以實現如下圖所示轉化關系的是
選項 | X | Y | Z | 對應過程的反應條件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①Na2CO3熔融 |
B | NaOH | NaHCO3 | Na2CO3 | ②加熱 |
C | N2 | NO2 | HNO3 | ③加熱 |
D | C | CO | CO2 | ④灼熱炭粉 |
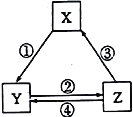
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com