
【題目】工業上真空煉銣的原理為2RbCl+Mg![]() MgCl2+2Rb(g),下列說法正確的是( )
MgCl2+2Rb(g),下列說法正確的是( )
A.鎂的金屬活動性比銣強,故鎂可置換銣
B.銣的沸點比鎂低,把銣蒸氣抽出時,平衡右移
C.MgCl2的熱穩定性比RbCl弱
D.Rb單質比RbCl更穩定
 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:
【題目】⑴氯堿工業是以惰性電極電解飽和食鹽水,制取氯氣、氫氣、燒堿和氯的含氧酸鹽等系列化工產品。下圖是離子交換膜法電解食鹽水的示意圖,圖中的離子交換膜只允許陽離子通過。
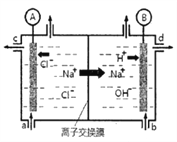
完成下列填空:
①離子交換膜的作用為:____________________。
②寫出電解飽和食鹽水的離子方程式_________。
③氫氧化鈉溶液從圖中_____位置流出。(選填a、b、c或d)
⑵電化學在日常生活中用途廣泛,圖①是鎂次氯酸鈉燃料電池,電池總反應為:Mg+ClO-+H2O===Cl-+Mg(OH)2↓,圖②是Cr2O![]() 的工業廢水的處理,下列說法正確的是(____)
的工業廢水的處理,下列說法正確的是(____)
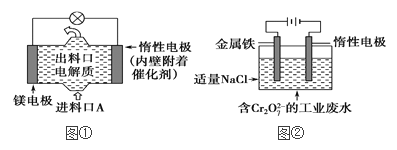
A.圖②中Cr2O![]() 離子向惰性電極移動,與該極附近的OH-結合轉化成Cr(OH)3除去
離子向惰性電極移動,與該極附近的OH-結合轉化成Cr(OH)3除去
B.圖②的電解池中,有0.084 g陽極材料參與反應,陰極會有33.6 mL的氣體產生
C.圖①中發生的還原反應是:Mg2++ClO-+H2O+2e-===Cl-+Mg(OH)2
D.若圖①中3.6 g鎂溶解產生的電量用以圖②廢水處理,理論可產生10.7 g氫氧化鐵沉淀
⑶觀察下列裝置,回答下列問題:
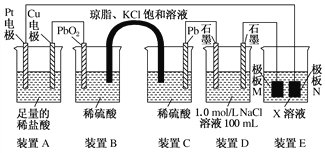
①裝置B中PbO2上發生的電極反應方程式為_____________________________________。
②裝置A中總反應的離子方程式為_____________________________________________。
③當裝置A中Cu電極質量改變6.4 g時,裝置D中產生的氣體體積為________ L(標準狀況下,不考慮氣體的溶解)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知傘形酮可用雷瑣苯乙酮和蘋果酸在一定條件下反應制得。
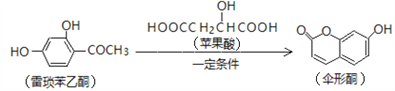
下列說法中正確的是
A. 1mol雷瑣苯乙酮最多能與3mol Br2發生取代反應
B. 蘋果酸能形成一種縮聚產物是![]()
C. 1mol傘形酮與足量NaOH溶液反應,最多可消耗2mol NaOH
D. 雷瑣苯乙酮、蘋果酸、傘形酮都能跟FeCl3溶液發生顯色反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物X是一種香料,可采用乙烯與甲苯為主要原料,按下列路線合成:

已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’ 請回答:
RCH=CHCOOR’ 請回答:
(1) A中官能團的名稱是______________________。
(2) D→E的化學方程式________________________________________________。
(3) X的結構簡式_________________。
(4)與F互為同分異構體又滿足下列條件的有_______種。
①遇到氯化鐵溶液會顯紫色,②會發生銀鏡反應 ③苯環上有三個取代基
在其它同分異構體中核磁共振氫譜有六組峰,氫原子數比符合1:2:2:2:2:1的結構為_____。
(5)根據上面合成信息及試劑,寫出以乙烯為原料(無機試劑任選),寫出合成CH3CH=CHCOOCH2CH3路線。_____________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖表示細胞內某些有機物的元素組成和功能關系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,圖中X、Y、Z、P分別為構成生物大分子的基本單位。請回答下列問題:
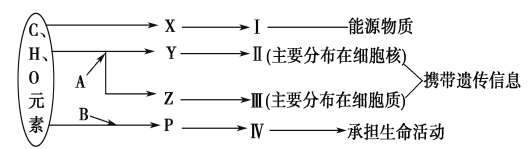
(1)圖中X是________,I在小麥種子中主要是指______________。
(2)圖中Z是________,使用甲基綠、派洛寧(吡羅紅)混合染液染色,可使Ⅲ呈現________色。
(3)圖中P的結構通式為________;寫出由P形成Ⅳ的結構層次______________。
(4)Ⅲ和Ⅳ兩者都有多樣性,兩者多樣性的關系是前者________后者。
(5)構成細胞的化合物中,隨著年齡增長明顯減少的主要是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】因在航空、核能、電池等高技術領域的重要作用——鋰被稱為“21世紀的能源金屬”。完成下列填空:
(1)鋰位于元素周期表的________。鋰的很多化學性質與鎂相似,請依據元素周期律進行解釋:_________。
(2)氫化鋰(LiH)是離子化合物,寫出其陰離子的電子式_______________,LiH中陰離子半徑大于陽離子半徑,其原因是__________________________________________________。
(3) 工業上用Li2CO3制取鋰的化合物及金屬鋰。碳原子核外電子有________種不同能量的電子,其中有兩個電子的能量最高且能量相等,這兩個電子所處的軌道是_____________________。
(4)用Li2CO3、氨水和液溴制備LiBr·H2O的流程如下:

①合成時,除生成LiBr外,還產生了兩種參與大氣循環的氣體,補全產物并配平該反應的化學方程式:
Li2CO3+Br2+ NH3·H2O→LiBr+(___) __________。
②溴化鋰的溶解度隨溫度變化曲線如圖所示,請補全從溶液中得到LiBr·H2O晶體的實驗步驟:_____、過濾、用乙醇洗滌,干燥。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z、W、L為五種短周期元素,非金屬元素X最外層電子數與其周期序數相同,Y的最外層電子數是其所在周期數的2倍。Y在Z中充分燃燒能生成其最高價化合物YZ2。W+與Z2-具有相同的電子數。X在L中燃燒,產物XL溶于水得到一種強酸。請回答下列問題:
(1)X在周期表中的位置是_____。請寫出實驗室制備單質L的化學方程式______,尾氣處理的離子方程式____________。
(2)由X分別與Y、Z形成的最簡單化合物的穩定性關系為___________________。
(3)由X、Y、Z、W組成的一種鹽,在面食中有大量使用,在其水溶液中滴入由X、Y、Z形成的廚房中常見的一種酸,反應的離子方程式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知化學反應A2(g)+B2(g)=2AB(g)的能量變化如圖所示,判斷下列敘述中正確的是()

A. 斷裂1 mol A—A和1 mol B—B鍵,放出a kJ能量
B. 每生成2 mol AB(g)吸收b kJ能量
C. 該反應中反應物的總能量高于生成物的總能量
D. 該反應熱ΔH=(a-b) kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】濃度均為0.1mol/L、體積為V0的HX、HY溶液,分別加水稀釋至體積V,pH隨lg(V/ V0)的變化關系如圖所示。下列敘述正確的是( )

A. HX、HY都是弱酸,且HX的酸性比HY的弱
B. 相同溫度下,電離常數K(HX):a>b
C. 常溫下,由水電離出的c(H+)·c(OH-):a<b
D. lg(V/ V0)=3,若同時微熱兩種溶液,則[c(X-)/c(Y-)]減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com