
【題目】Ⅰ.下表是元素周期表的一部分,表中所列的字母分別代表某一化學元素。

(1)下列___________ (填寫編號)組成元素的單質可能都是電的良導體。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)如果給核外電子足夠的能量,這些電子便會擺脫原子核的束縛而離去。核外電子離開該原子或離子所需要的能量主要受兩大因素的影響:
A.原子核對核外電子的吸引力
B.形成穩定結構的傾向。
Ⅱ.下表是一些氣態原子失去核外不同電子所需的能量(kJ·mol-1):
鋰 | X | Y | |
失去第一個電子 | 519 | 502 | 580 |
失去第二個電子 | 7 296 | 4 570 | 1 820 |
失去第三個電子 | 11 799 | 6 920 | 2 750 |
失去第四個電子 | 9 550 | 11600 |
①通過上述信息和表中的數據分析為什么鋰原子失去核外第二個電子所需的能量遠遠大于失去第一個電子所需的能量。
____________________________。
②表中X可能為以上13種元素中的__________ (填寫字母)元素。用元素符號表示X和j形成化合物的化學式: __________。
③Y是周期表中__________族元素。
④以上13種元素中, __________ (填寫字母)元素原子失去核外第一個電子需要的能量最多。
【答案】(1)①④(2分,對一個得1分,錯一個扣1分,扣完為止)
(2)①Li原子失去一個電子后,Li+已形成穩定結構,此時再失去一個電子很困難(2分)
②a(1分);![]() (2分);離子(1分)
(2分);離子(1分)
③ⅢA(或第三主族)(1分)
④m(1分)
【解析】試題分析:a-m元素分別為Na、H、Mg、Ba、Ti、Al、Ge、C、P、O、Te、Cl、Ar。(1)電的良導體主要為金屬、石墨、人體、大地以及酸、堿、鹽的水溶液等。(2)元素X失去第一個電子所需能量遠遠小于失去第二個電子所需的能量,故X元素位于第一主族,為Na;與j形成的化合物有Na2O和Na2O2,其中Na2O2含有共價鍵;m為稀有氣體元素,已達穩定結構,故很難失去電子。


科目:高中化學 來源: 題型:
【題目】高一入學體檢時,小明體檢的血液化驗單中,出現了如下圖所示的體檢指標。表示該體檢指標的物理量是( )
甘油三酯 0.52 mmol/L 總膽固醇 4.27 mmol/L 高密度脂蛋白膽固醇 1.57 mmol/L 低密度脂蛋白膽固醇 1.40 mmol/L 葡萄糖 4.95 mmol/L |
A.溶解度 B.物質的量濃度
C.質量分數 D.摩爾質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合理應用和處理含氮的化合物,在生產生活中有重要意義。
(1)用活化后的V2O5作催化劑,氨氣將NO還原成N2的一種反應歷程如圖1所示。

寫出總反應化學方程式 。
(2)已知N2(g)+3H2(g)![]() 2NH3(g) △H=-94.4gKJ·mol-1,恒容時,體系中各物質濃度隨時間變化的曲線如圖2所示。
2NH3(g) △H=-94.4gKJ·mol-1,恒容時,體系中各物質濃度隨時間變化的曲線如圖2所示。

在2L容器中發生反應,前20min內,v(NH3)= ,放出的熱量為 。
25min時采取的措施是 。
③時段III條件下,反應的平衡常數表達式為 (只列計算表達式,不計算)。
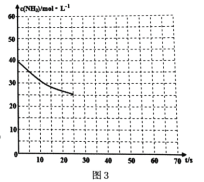
(3)用氨氣制取尿素[CO(NH2)2]的反應:2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(g);△H<0。某溫度下,向容器為0.1L的密閉容器中通入4molNH3和2molCO2,該反應進行到40s時,達到平衡,此時CO2的妝花率為50%。圖3中的曲線表示在前25s內NH3的濃度隨時間的變化而變化。其他條件不變,請在圖3中用實線畫出使用催化劑后c(NH3)隨時間的變化曲線。
CO(NH2)2(s)+H2O(g);△H<0。某溫度下,向容器為0.1L的密閉容器中通入4molNH3和2molCO2,該反應進行到40s時,達到平衡,此時CO2的妝花率為50%。圖3中的曲線表示在前25s內NH3的濃度隨時間的變化而變化。其他條件不變,請在圖3中用實線畫出使用催化劑后c(NH3)隨時間的變化曲線。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞砜(SOCl2)是一種很重要的化學試劑,可以作為氯化劑和脫水劑。下列關于氯化亞砜分子的幾何構型和中心原子( S )采取雜化方式的說法正確的是( )
A. 三角錐型、sp3 B. V形、sp3 C. 平面三角形、sp2 D. 三角錐型、sp2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機反應的說法正確的是( )
A. 丙烯能與氫氣發生加成反應,而苯不能
B. 乙烯和聚乙烯都可與溴水發生加成反應
C. 乙酸和乙醇發生酯化反應的反應機理是酸脫羥基醇脫氫
D. 甲烷和Cl2的反應和乙烯和Br2的反應屬于同一反應類型
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于液氯和氯水的敘述中正確的是( )
A.液氯是純凈物,而氯水是混合物
B.液氯有酸性,氯水有漂白性
C.液氯較氯水的漂白作用更強
D.液氯無色,氯水呈黃綠色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com