
【題目】除去Na2CO3 固體中少量NaHCO3的最佳方法是
A.加入適量鹽酸 B.加熱 C.加入NaOH溶液 D.配成溶液后通入CO2
 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:
【題目】硫是一種生命元素,組成某些蛋白質時離不開它。SO2是硫的一種重要氧化物,為探究SO2的性質,某化學興趣小組的同學進行如下系列實驗:
(1)將SO2通入紫色石蕊試液,現象是_________________。
(2)將SO2通入FeCl3溶液中,使其充分反應。寫出SO2與FeCl3反應的離子方程式___________________;為了驗證SO2與FeCl3發生了氧化還原反應,將反應后的溶液分成兩份,并設計如下實驗:
方案1:往第一份試液中加入少量酸性KMnO4溶液,紫紅色褪去;
方案2:往第二份試液中加入KSCN溶液,不變紅,再加入新制氯水,溶液變紅。
上述方案合理的是__________。(填“方案1”或“方案2”或“均合理”)
(3)將SO2通入到BaCl2溶液中,出現了異常現象,看到了明顯的白色沉淀。為探究該白色沉淀的成分,他們設計了如下實驗流程:

操作①的名稱為_____,試劑A為_______:加入試劑A后,白色沉淀未見溶解,則該白色沉淀的成分是_______(填化學式)。
(4)為探究SO2的漂白是SO2直接作用于有色物質還是SO2與水反應的產物的作用。設計如圖裝置進行探究。
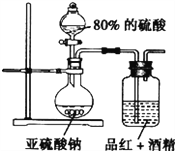
(信息提示:品紅能溶解在酒精中形成紅色溶液;H2SO3是二元弱酸)
①亞硫酸鈉和濃硫酸反應的化學方程式為__________。
②請指出設計的裝置中兩個明顯的不足:
___________________;________________________。
③按照修改后的裝置,實驗中控制SO2以較緩慢的速率通過品紅的酒精溶液,60分鐘后溶液仍不褪色,由此可推斷,引起品紅褪色的微粒可能是______________(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合金貯氫材料具有優異的吸放氫性能,在配合氫能的開發中起到重要作用。
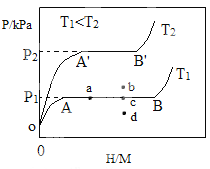
(1)一定溫度下,某貯氫合金(M)的貯氫過程如圖所示,縱軸為平衡時氫氣的壓強(p),橫軸表示固相中氫原子與金屬原子的個數比(H/M)。在OA段,氫溶解于M中形成固溶體MHx,隨著氫氣壓強的增大,H/M逐慚增大;在AB段,MH與氫氣發生氫化反應生成氫化物MHy,氫化反應方程式為:zMHx(s)+H2(g)![]() zMHy(s) △H1(I);B點,氫化反應結束,進一步增大氫氣壓強,H/M幾乎不變。
zMHy(s) △H1(I);B點,氫化反應結束,進一步增大氫氣壓強,H/M幾乎不變。
反應(I)的焓變△HⅠ_______0(填“>”“<”或“=”)。
反應(I)中z=___________(用含x和y的代數式表示)。
溫度為T1時,2g某合金4min內吸收氫氣240mL,吸氫速率v=________mLg1min1。
(2)當反應(I)處于圖中a點時,保持溫度不變,向恒容體系中通入少量氫氣,達到平衡后反應(I)可能處于圖中的_______點(填“b”“c”或“d”),該貯氫合金可通過______或_______的方式釋放氫氣。η表示單位質量貯氫合金在氫化反應階段的最大吸氫量占其總吸氫量的比例,則溫度為T1、T2時,η(T1)___ _______η(T2)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如圖所示。已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的單質是一種常見的半導體材料;Z的非金屬性在同周期主族元素中最大。
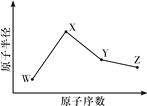
(1)X位于元素周期表中的位置是____________________。
(2)Z的氣態氫化物和溴化氫相比,較穩定的是____________(寫化學式)。
(3)W與X形成的一種化合物和水反應能生成W的單質,請寫出該反應的化學方程式:________________________________________________________________________。
(4)Y與Z形成的化合物和足量水反應,生成一種弱酸和一種強酸,該反應的化學方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】糖類、脂肪和蛋白質是維持人體生命活動所必需的三大營養物質。以下敘述正確的是
A.植物油不能使溴的四氯化碳溶液褪色
B.葡萄糖能發生氧化反應和水解反應
C.麥芽糖水解的最終產物是葡萄糖
D.蛋白質溶液遇硫酸銅后產生的沉淀能重新溶于水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對制取水泥和玻璃的共同特點的敘述中,錯誤的是
A. 生產設備相同 B. 原料中均有石灰石
C. 反應都在高溫下進行 D. 發生的都是復雜的物理化學變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室里用二氧化錳和濃鹽酸加熱制取氯氣;
(1)該反應的離子方程式為____________________________。
根據反應原理,圖乙中合適的氣體發生裝置為 ______ 。
(2)也可以利用反應2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O制取并收集純凈、干燥的氯氣,部分裝置如圖甲所示。
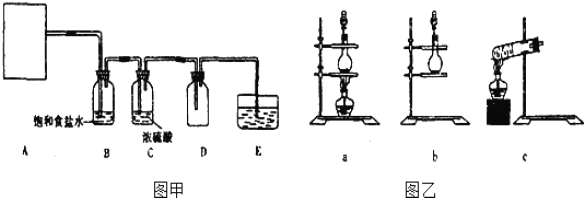
根據反應原理,圖乙中合適的制氣裝置為 ______ 。
(3)裝置B的作用是 ______ 。
(4)裝置E的作用是 ______,E中的試劑可選 ______ 。
A.NaOH溶液 B.NaCl溶液 C.澄清石灰水 D.水
(5)某同學通過下列兩種方式制取氯氣:
①用8.7g MnO2與足量濃鹽酸反應;
②用含14.6g HCl的濃鹽酸與足量MnO2反應這兩種方式產生Cl2的量的關系是 ______。
A.①多 B.②多 C.一樣多 D.不確定.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學實驗能夠獲得成功的是( )
A. 只用溴水為試劑, 可以將苯、乙醇、己烯、四氯化碳四種液體區分開來。
B. 將無水乙醇加熱到 170℃時, 可以制得乙烯
C. 苯酚和福爾馬林在沸水浴中加熱可以制取酚醛樹脂
D. 乙醇、冰醋酸和 2 mol/L 的硫酸混合物, 加熱可以制備乙酸乙酯。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的敘述符合事實的是
A. 乙烯使溴水和酸性高錳酸鉀溶液褪色的反應都屬于氧化反應
B. 乙酸和乙醇均能與NaOH溶液發生反應
C. 苯與溴水混合后加入FeBr3做催化劑,可發生取代反應生成溴苯
D. C5H11Br有8種同分異構體,它們的熔點、沸點各不相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com