
【題目】工業上由黃銅礦(主要成分為 CuFeS2)冶煉銅的主要流程如下。下列說法不正確的是
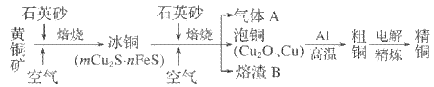
A. 氣體A中的大氣污染物可用氨水吸收并回收利用
B. 由泡銅冶煉粗銅的化學方程式為3Cu2O+2Al ![]() Al2O3+6Cu
Al2O3+6Cu
C. 加入石英砂作為添加劑熔劑,生成更穩定、更容易分離的硅酸鹽
D. 用過量稀H2SO4可全部溶解熔渣B
 導學全程練創優訓練系列答案
導學全程練創優訓練系列答案科目:高中化學 來源: 題型:
【題目】最早使用的化學電池是鋅錳電池,即大家熟悉的干電池,其結構如圖所示。

盡管這種電池的歷史悠久,但對于它的化學過程人們尚未完全了解。一般認為,放電時,電池中的反應如下:
E極:2MnO2+2e-+2NH4+===Mn2O3+H2O+2NH3↑
F極:Zn-2e-===Zn2+
總反應式:2MnO2+Zn+2NH4+===Mn2O3+Zn2++2NH3↑+H2O
下列說法正確的是
A.E極是電池的正極,發生的是氧化反應
B.F極是電池的負極,發生的是氧化反應
C.從結構上分析,鋅錳電池應屬于可充電電池
D.鋅錳電池內部發生的氧化還原反應是可逆的
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、C、D、E、F、G7種物質的轉化關系如下:
(1)A+B→C+H2O (2)C+KOH→D↓(藍色)+E
(3) B+D→C+H2O (4)E+BaCl2→KCl + F↓(白色,不溶于稀硝酸)
(5)G+B→CO2↑+F↓+H2O,反應中B與CO2的物質的量之比為1:2
根據上述變化關系填空:
(1)請寫出下列物質的化學式:B___;C___;F___;G___。
(2)檢驗E中的陰離子的實驗是___。
(3)往G的溶液中滴加過量的KOH,反應的離子方程式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物M在模擬酶用于可視化生物硫醇檢驗中起到重要的作用,結構簡式如下圖。有關M的說法不正確的是
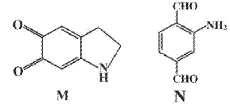
A. 分子式為C8H7NO2
B. 可發生取代反應、加成反應、氧化反應
C. 分子中所有碳原子都在同一平面上
D. 有機物N是M的同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據報道,美國正在研究的鋅電池可能取代目前廣泛使用的鉛酸蓄電池。鋅電池具有容量大、污染少等優點。電池反應為2Zn+O2=2ZnO,原料為鋅粒、電解液和空氣。下列敘述正確的是( )
A. 鋅為正極,空氣進入負極反應B. 負極反應為Zn+2OH--2e-=ZnO+H2O
C. 正極發生氧化反應D. 電解液可以是乙醇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為除去粗鹽中的Ca2+、Mg2+、SO![]() 以及泥沙等雜質,某同學設計了一種制備精鹽的實驗方案,步驟如下:(用于沉淀的試劑稍過量)
以及泥沙等雜質,某同學設計了一種制備精鹽的實驗方案,步驟如下:(用于沉淀的試劑稍過量)
稱取粗鹽![]()
![]()
![]()
![]()
![]() 濾液
濾液![]()
![]() 精鹽
精鹽
(1)第①步中,操作A是________,第⑤步中,操作B是________。
(2)第④步中,寫出相應的化學方程式(假設粗鹽溶液中Ca2+的主要存在形式為CaCl2)_______。
(3)若先用鹽酸調pH再過濾,將對實驗結果產生影響,其原因是__________________。
(4)判斷BaCl2已過量的方法是___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+、Na+。某同學為了確認其成分,取部分試液,設計并完成了如下實驗:
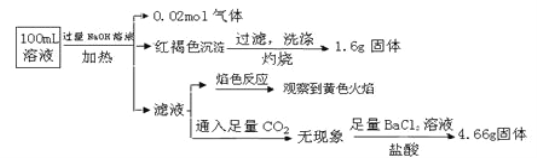
下列說法正確的是( )
A. 原溶液中c(Fe3+)=0.2 molL-1
B. 溶液中至少有4種離子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
C. SO42-、NH4+、Na+、CO32-一定存在,Cl-可能存在
D. 要確定原溶液中是否含有Fe2+,其操作為:取少量原溶液于試管中,加入適量氯水,無現象,再加KSCN溶液,溶液成血紅色,則含有Fe2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為2L的恒容密閉容器中發生反應xA(g)+ yB(g)![]() zC(g),圖I表示200℃時容器中A、B、C物質的量隨時間的變化,圖Ⅱ表示不同溫度下平衡時C的體積分數隨起始n(A):n(B)的變化關系;則下列結論正確的是
zC(g),圖I表示200℃時容器中A、B、C物質的量隨時間的變化,圖Ⅱ表示不同溫度下平衡時C的體積分數隨起始n(A):n(B)的變化關系;則下列結論正確的是

A. 圖II所知反應xA(g)+yB(g) ![]() zC(g) △H<0,且a=2
zC(g) △H<0,且a=2
B. 200℃時,該反應的平衡常數為25
C. 200℃時,反應從開始到平衡的平均速率v(B)=0.04mol/(Lmin)
D. 當外界條件由200℃降溫到100℃,平衡正向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應2NO2![]() 2NO+O2在恒容密閉容器中進行,達到平衡狀態的標志是
2NO+O2在恒容密閉容器中進行,達到平衡狀態的標志是
①單位時間生成n mol O2,同時生成2n mool NO ②單位時間內生成n mol O2,同時生成2n mol NO2 ③用NO2、NO、O2的物質的量濃度變化表示的反應速率的比為2∶2∶1 ④混合氣體的顏色不再改變 ⑤混合氣體的密度不再改變 ⑥混合氣體的平均相對分子質量不再改變
A. ①③⑤ B. ②④⑥ C. ②③④ D. ③④⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com