
下列離子方程式書寫正確的是
| A.將銅屑加入Fe3+溶液中:Fe3++Cu=Fe2++Cu2+ |
B.NH4HCO3溶液與過量KOH濃溶液共熱:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.稀硝酸和過量的鐵屑反應:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
| D.KI溶液與H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+ =2H2O+I2 |
D
解析試題分析:鐵元素由+3降為+2價,銅元素由0升高為+2價,則鐵元素化合價降低數為1,銅元素化合價升高數為2,因此得失電子不守恒;等號左邊物質帶3個正電荷,右邊物質帶4個正電荷,因此左右電荷不守恒,所以該反應沒有配平,銅屑加入鐵鹽溶液中的反應為2Fe3++Cu=2Fe2++Cu2+,故A錯誤;由于KOH過量,不僅銨根離子與氫氧根離子能完全反應,而且碳酸氫根離子與氫氧根離子也能完全反應,不能漏寫離子反應,則碳酸氫銨溶液與氫氧化鉀溶液共熱的反應為NH4++HCO3-+2OH- NH3↑+CO32-+2H2O,故B錯誤;鐵離子具有氧化性,鐵具有還原性,則鐵離子與過量的單質鐵能繼續發生氧化還原反應,生成亞鐵離子,不能違反這個客觀反應事實,也不能違反電荷守恒原理,所以稀硝酸和過量的鐵屑反應為3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C錯誤;碘離子具有還原性,過氧化氫在酸性條件下具有氧化性,二者能發生氧化還原反應,生成單質碘和水,該反應式符合客觀反應事實,也符合電子守恒、電荷守恒、原子守恒,故D正確。
NH3↑+CO32-+2H2O,故B錯誤;鐵離子具有氧化性,鐵具有還原性,則鐵離子與過量的單質鐵能繼續發生氧化還原反應,生成亞鐵離子,不能違反這個客觀反應事實,也不能違反電荷守恒原理,所以稀硝酸和過量的鐵屑反應為3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C錯誤;碘離子具有還原性,過氧化氫在酸性條件下具有氧化性,二者能發生氧化還原反應,生成單質碘和水,該反應式符合客觀反應事實,也符合電子守恒、電荷守恒、原子守恒,故D正確。
考點:考查離子方程式,涉及氧化還原反應、復分解反應、過量反應物與生成物繼續反應等。


 能考試期末沖刺卷系列答案
能考試期末沖刺卷系列答案科目:高中化學 來源: 題型:單選題
在指定條件下,下列各組離子可能大量共存的是
A.無色澄清透明溶液中: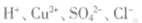 |
B.與鋁反應放出H2的溶液中: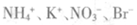 |
C.滴加酚酞顯紅色有溶液中: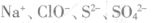 |
D.由水電離的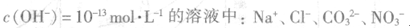 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,下列各組離子在指定溶液中一定能大量共存的是
| A.0.1 mol·L-1的NaI溶液:K+、H+、SO42-、NO3- |
| B.0.1 mol·L-1的NaHCO3溶液:K+、Na+、NO3-、Cl- |
| C.0.1 mol·L-1 FeCl3溶液:K+、Na+、ClO-、Cl- |
| D.0.1 mol·L-1的氨水:Cu2+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列離子方程式正確的是
| A.氨水吸收足量的SO2氣體:OH-+SO2=HSO3- |
| B.稀硝酸中加入過量鐵粉: Fe + 4H++ NO3-=Fe3++ NO↑ + 2H2O |
| C.用NaOH溶液吸收廢氣中氮氧化物:NO+NO2+OH-=NO2-+H2O |
D.苯酚鈉溶液中通入少量CO2: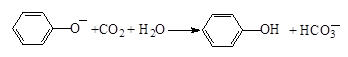 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
水溶液中能大量共存的離子組是
| A.Fe3+、Na+、SO42-、Cl- |
| B.H+、Fe2+、Cl-、NO3- |
| C.Ag+、Na+、CO32-、NO3- |
| D.Al3+、K+、Cl-、AlO2- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列離子方程式正確的是
| A.氫氧化鎂與稀鹽酸反應:H+ + OH-=H2O |
| B.AlCl3溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ |
| C.銅溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D.次氯酸鈣溶液中通入過量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列溶液中,各組離子一定能大量共存的是
| A.能使石蕊試液呈藍色的溶液:Na+、I-、Cl-、NO3- |
| B.含大量Fe3+的溶液:NH4+、Na+、Cl-、SCN- |
| C.能與Al反應生成H2的溶液:Ca2+、NH4+、HCO3-、Cl- |
| D.水電離出的c(H+)=1×10-14mol/L的溶液:K+、AlO2-、Br-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在酸性溶液中,下列各組離子能大量共存且溶液為無色透明的是
| A.Na+、K+、OH-、Cl- | B.Na+、Cu2+、SO42-、NO3- |
| C.Mg2+、Na+、SO42-、Cl- | D.K+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列離子方程式書寫正確的是
| A.硫氫化鈉的水解:HS-+H2O === S2-+H3O+ |
| B.Fe(OH)3溶于氫碘酸中:Fe(OH)3+3H+=== Fe3++3H2O |
| C.鋼鐵發生吸氧腐蝕的負極反應式:O2+4e-+2H2O === 4OH- |
| D.碳酸氫銨溶液中滴入少量燒堿溶液:HCO3-+OH-=== CO32-+H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com