
科目:高中化學 來源: 題型:
【題目】下列示意圖與對應的反應情況正確的是
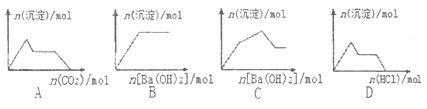
A. 含0.01molKOH和0.01molCa(OH)2的混合溶液中緩慢通入CO2
B. NaHSO4溶液中逐滴加入Ba(OH)2溶液
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
D. Na[Al(OH)4]溶液中逐滴加入鹽酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖,某氣體X可能由H2、CO、CH4中的一種或幾種組成.將X氣體燃燒,把燃燒后生成的氣體通過A、B兩個洗氣瓶.試回答下列問題: 
(1)若A洗氣瓶的質量增加,B洗氣瓶的質量不變,則氣體X是 .
(2)若A洗氣瓶的質量不變,B洗氣瓶的質量增加,則氣體X是 .
(3)若A、B兩個洗氣瓶的質量都增加,則氣體X可能是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知(1)H2O(g) = H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) = CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) = 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1
(Q1、Q2、Q3均大于0)若要使1mol液態甲醇完全燃燒,最后恢復到室溫,放出的熱量為(單位:kJ)( )
A. Q1+ Q2 + Q3 B. 0.5Q3-Q2+2Q1 C. Q3-2Q2+4Q1 D. 0.5(Q1+Q2+Q3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】目前人類已發現幾千萬種物質,對物質進行分類,有利于我們的學習。對于H2SO4分類不合理的是( )
A. 酸 B. 含氧酸 C. 無氧酸 D. 強酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知一定條件下合成氨反應:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,在反應過程中,反應速率的變化如圖所示,請根據速率的變化回答采取的措施。
2NH3(g) ΔH=-92.4 kJ·mol-1,在反應過程中,反應速率的變化如圖所示,請根據速率的變化回答采取的措施。
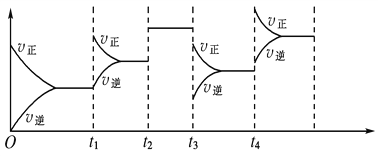
t1________________; t2______________; t3________________; t4______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,下列可逆反應達到化學平衡:2NO2 (g) ![]() N2O4 (g) ,ΔH < 0,要使混合氣體的顏色加深,可以采取的方法是( )
N2O4 (g) ,ΔH < 0,要使混合氣體的顏色加深,可以采取的方法是( )
A. 降低溫度 B. 充入適量N2
C. 縮小體積,增大壓強 D. 增大體積,減小壓強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.(1)25℃、101kPa時,使1.0 g乙烯與足量的氧氣反應,生成CO2和液態H2O并放出50 KJ的熱量,表示乙烯燃燒熱的熱化學方程式為_________________________。
(2)比較下列熱化學方程式中ΔH的大小關系。
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (l) ΔH1
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (g) ΔH2
則ΔH1________ΔH2
(3)依據蓋斯定律可以對某些難以通過實驗直接測定的化學反應的焓變進行推算。
已知:C (s,石墨) + O2 (g) = CO2 (g) ΔH1
2H2 (g) + O2 (g ) =2H2O (l) ΔH2
2C2H2 (g) + 5 O2 (g ) =4 CO2 (g)+2 H2O (1) ΔH3
則2C (s,石墨)+ H2 (g)= C2H2 (g) 反應的ΔH的表達式為:ΔH =_____。
II. 草酸與高錳酸鉀在酸性條件下能夠發生如下反應:2MnO4-+ 5H2C2O4+ 6H+= 2 Mn2++ 10CO2↑ + 8H2O。現用4 mL 0.001 mol/L KMnO4溶液與2 mL 0.01 mol/L H2C2O4溶液,研究不同條件對化學反應速率的影響。改變的條件如下:
組別 | 10%硫酸體積/mL | 溫度/℃ | 其他物質 |
I | 2 mL | 20 | / |
II | 2 mL | 20 | MnSO4固體 |
III | 2 mL | 30 | / |
IV | 1 mL | 20 | 1 mL蒸餾水 |
(4)如果研究催化劑對化學反應速率的影響,使用實驗_______和____ (用I~IV表示,下同);如果研究溫度對化學反應速率的影響,使用實驗_____和______。
(5)對比實驗I和IV,可以研究_________________對化學反應速率的影響,實驗IV中加入1 mL蒸餾水的目的是 _______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com