
【題目】下表是元素周期表的一部分, 針對表中的①~⑩種元素,填寫下列空白:[
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)在最高價氧化物的水化物中,酸性最強的化合物的分子式是: ,堿性最強的化合物的電子式是: 。
(2)最高價氧化物是兩性氧化物的元素是 ;寫出它的氧化物與氫氧化鈉反應的離子方程式 。
(3)用電子式表示元素④與⑥的化合物的形成過程: 。
(4)表示①與⑦的化合物的電子式 ,該化合物是由 (填“極性”“非極性”)鍵形成的。
(5)③、⑥、⑦三種元素形成的離子,離子半徑由大到小的順序是_______(要求用離子符號表示)。
(6)元素③的氫化物常溫下和元素⑦的單質反應的離子方程式為: 。
【答案】(1)HClO4;![]()
(2)Al;Al2O3+2OH-=2AlO2-+H2O。
(3)![]()
(4)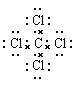 ;極性共價鍵
;極性共價鍵
(5)S2->Cl->O2-(6)Cl2+H2O=H++Cl-+HClO。
【解析】試題分析:根據元素在周期表中的位置可知①~⑩種元素分別是C、N、O、Na、Al、S、Cl、Ar、K、Br。
(1)在最高價氧化物的水化物中,酸性最強的化合物的分子式是HClO4,堿性最強的化合物是氫氧化鉀,含有離子鍵和共價鍵,電子式為![]() 。
。
(2)最高價氧化物是兩性氧化物的元素是Al,它的氧化物與氫氧化鈉反應的離子方程式為Al2O3+2OH-=2AlO2-+H2O。
(3)元素④與⑥形成的化合物是硫化鈉,含有離子鍵,其形成過程為![]() 。
。
(4)①與⑦形成的化合物是四氯化碳,含有共價鍵,電子式為 ,該化合物是由極性鍵形成的。
,該化合物是由極性鍵形成的。
(5)離子的核外電子層數越多,離子半徑越大,核外電子排布相同的離子,離子半徑隨原子序數的增大而減小,則③、⑥、⑦三種元素形成的離子,離子半徑由大到小的順序是S2->Cl->O2-。
(6)元素③的氫化物常溫下和元素⑦的單質反應的離子方程式為Cl2+H2O=H++Cl-+HClO。


科目:高中化學 來源: 題型:
【題目】生物學家借助新的顯微技術,成功觀察到小于200納米的粒子。下列分散系中,分散質粒子半徑最小的是( )
A.霧 B.蛋白質溶液 C.石灰乳 D.KNO3溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.下圖所示為實驗室常見氣體制備、凈化、干燥、收集和性質等實驗所用到的部分儀器,某校化學興趣小組利用這些儀器進行實驗探究,請你參與實驗并完成有關問題:
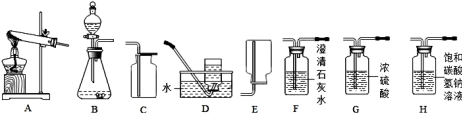
(1)甲組同學用加熱高錳酸鉀的方法制取氧氣,應選擇的發生裝置為 (填字母序號);若他們選用D裝置來收集O2,當氣體收集滿后,從水槽中取出集氣瓶的操作為 。
(2)乙組同學以石灰石和稀鹽酸為原料,制備并收集一瓶干燥、純凈的二氧化碳氣體,按要求設計實驗裝置、連接儀器、并檢驗裝置的氣密性、所選儀器的連接順序應為: → → → ;請用離子方程式表示H瓶中飽和NaHCO3溶液的作用: ;若將少量二氧化碳氣體通入澄清石灰水中,發生反應的離子方程式為 。
Ⅱ.某校化學實驗室有四瓶失去標簽的溶液,分別標為A、B、C、D,已知它們是碳酸鈉溶液、氯化鋇溶液、硫酸鈉溶液和稀鹽酸中的一種。該校化學興趣小組的同學進行以下實驗探究來鑒別這四種溶液。
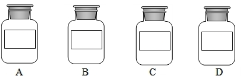
(3)丙同學的實驗操作如圖1所示,由此你推斷該同學認為A一定不是 ;然后他再接著向實驗后的混合溶液中滴加酚酞試液,發現混合溶液由無色變為紅色,則丙同學得出結論:A一定是氯化鋇溶液。
(4)丁同學則不同意丙同學的結論,你認為丁同學的理由是 ;于是丁同學另取少量A于試管中,向其中滴加一種試劑為 (注:只能從下列備選試劑中選擇一種!),根據所選試劑他應該觀察到的明顯現象為 ;
A.飽和食鹽水 B.K2CO3溶液 C.蒸餾水 D.紫色石蕊試液
由此證明了丙同學的結論是錯誤的;同時也確定了A的成分。
(5)戊同學的實驗操作如圖2所示,實驗時觀察到C中產生氣泡,D中產生白色沉淀。寫出D中發生反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用甲和乙通過化合反應制備丙,如圖是三種分子的模型圖,根據微觀示意圖得出的結論錯誤的是
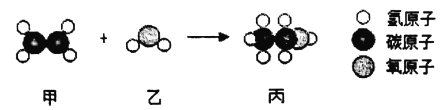
A.甲的化學式為C2H4
B.保持乙化學性質的最小微粒是水分子
C.化學反應前后分子的種類都發生了改變
D.乙和丙都屬于氧化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是一種清潔能源,又是合成氨工業的重要原料。
(1)已知:CH4(g)+H2O==CO+3H2(g) △H=206.2 kJ·mol-1。
CH4(g)+CO2(g)==2CO(g)+2H2(g) △H=247.4 kJ·mol-1
甲烷和H2O(g)反應生成H2和CO2的熱化學方程式為___________________。
(2)工業合成氨的反應原理為N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ·mol-1。
2NH3(g) △H=-92.4 kJ·mol-1。
某溫度下,把10 mol N2與28 mol H2置于容積為10 L的密閉容器內,10 min時反應達到平衡狀態,測 得氮氣的平衡轉化率為60%,則10 min內該反應的平均速率v(NH3)=__________mol·L-1·min-1,該溫度下該反應的平衡常數K=________。 欲增大氮氣的平衡轉化率,可采取的措施有_____________、____________等(共寫兩條措施即可,每空一條)。
(3)下圖所示裝置工作時均與H2有關。
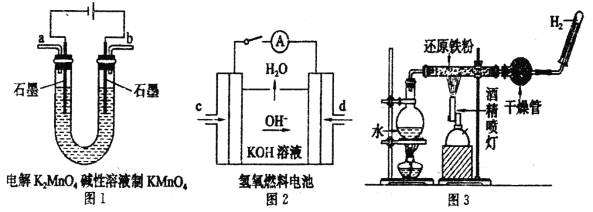
圖l所示裝置中陽極的電極反應式為______________。
②圖2所示裝置中,通入H2的管口是_____________(選填字母代號)。
③某同學按圖3所示裝置進行實驗,實驗結束后.將玻璃管內固體物質冷卻后,溶于稀硫酸,充分反應后,滴加KSCN溶液。溶液不變紅,再滴入新制氯水,溶液變為紅色。該同學據此得出結論:鐵與水蒸氣反應生成FeO和H2。該結論_____________(填“嚴密”或“不嚴密”),你的理由是(用離子方程式和必要的文字說明)______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,是工業制硫酸的主要反應之一。
2SO3(g) ΔH<0,是工業制硫酸的主要反應之一。
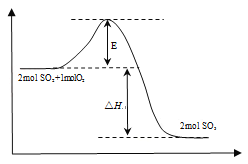
(1)該反應過程的能量變化如右圖所示:E的大小對該反應的反應熱有無影響_______(填“有”或“無”),該反應通常用V2O5作催化劑,加入V2O5后,改變的是圖中的_______。
A.△H B.E C.△H – E D.△H + E
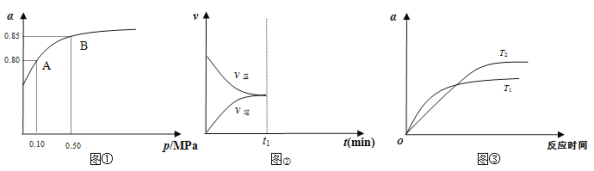
(2)某溫度下,甲同學將2 mol SO2和1 mol O2置于密閉容器中,反應達平衡后,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖①所示,若A點二氧化硫的平衡濃度為0.04 mol/L,則容器的體積為_______L;圖①中B點SO2、O2、SO3的平衡濃度之比為________________;反應到達平衡時,時間t1時縮小容器體積,請在圖②中畫出時間t1之后反應速率變化圖像;圖③為壓強等于0.50 MPa時不同溫度下SO2轉化率與溫度關系圖,圖中T2_____T1(填寫“大于”或“小于”)
(3)在2 L的密閉容器中,乙同學投入2 mol SO2和b mol O2,25 min時達到平衡,如下圖所示,在35 min時,改變某一條件,經過一段時間后,70 min時,反應再次達到平衡,回答下列問題:
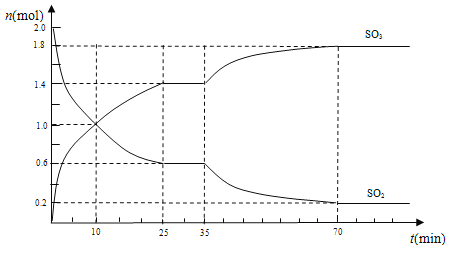
①10 min時,v(SO2)正________v(SO3)逆(填“>”“<”或“=”)
②求0~10 min時,v(O2)=______________
③反應開始至35 min時,測得反應共放熱138.6 kJ,則反應2SO2(g)+O2(g)![]() 2SO3(g)△H=____kJ/mol
2SO3(g)△H=____kJ/mol
④35 min時,改變的條件可能是___________________
a.加入更多的V2O5
b.從容器中分離出少量O2
c.投入一定量的SO3
d.降低反應溫度
e.往容器中加入N2,使容器壓強增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A + B → X + Y + H2O(未配平,反應條件略去)是中學常見反應的化學方程式,請回答:
(1)若Y為黃綠色氣體:
①當 A、B的物質的量之比為1∶4且A為黑色固體時,該反應的離子方程式是
;
②當 A、B的物質的量之比為1∶6時,寫出該反應的化學方程式,并用雙線橋表示反應過程中的電子轉移:_________________________________________。
(2)若A為單質,B為無色油狀黏稠液體,當 A、B的物質的量之比為1∶2時,則A可能為______________,檢查其中刺激性氣體產物X的方法是____________________。
(3)常溫下A在B的濃溶液中會“鈍化”,且A可溶于X溶液中,若A為金屬單質,A和B以物質的量之比1∶4反應。過量的A和100mL,2mol/L的B溶液充分反應后,將溶液稀釋至500mL,溶液中陰離子的物質的量濃度為______ _______。
(4)若A、B、X、Y均為化合物,向A溶液中加入硝酸酸化的AgNO3溶液,產生白色沉淀;B的焰色為黃色,則A與B按物質的量之比1:4反應后,溶液中溶質的化學式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com