
現有①鐵片 ②NaCl溶液 ③氨水 ④醋酸 ⑤酒精 ⑥鹽酸 ⑦H2SO4
⑧KOH固體 ⑨蔗糖 ⑩KAl(SO4)2·12H2O,其中能導電的是 ,屬于電解質的是____ ___,屬于非電解質的是 ,屬于酸的是 ,屬于堿的是 。(填序號)
科目:高中化學 來源: 題型:填空題
某工業廢水僅含下表中的某些離子,且各種離子的物質的量濃度相等,均為0.1 mol/L(此數值忽略水的電離及離子的水解)。
| 陽離子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 陰離子 | Cl- CO32— NO3— SO42— SiO32— I- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
根據要求回答下列各題
(Ⅰ)現有 ①鋁 ②NH3③氫氧化鈉溶液 ④液態氯化氫 ⑤AgCl固體⑥冰醋酸 ⑦蔗糖,填空回答(填序號):
以上物質中(1)屬于電解質的是 ;(2)屬于非電解質的是 ;
(3)屬于強電解質的是 ;(4)能導電的是 。
(Ⅱ)寫出下列反應的化學方程式:
①有NaHCO3生成的化合反應
② 有MgCl2參加的分解反應
③ 有Fe2O3參加的置換反應
④ 有HNO3生成的復分解反應
(Ⅲ).同溫同壓條件下,同體積的CH4和SO2的質量之比是 ;同質量的CH4和SO2的體積之比是 ;若兩者所含原子個數總數相等,則CH4和SO2的質量之比是 。
(Ⅳ)把鐵片和石墨棒用下列a、b兩種方式放在盛有稀硫酸鈉溶液和酚酞試液混合溶液的玻璃器皿中,經過一段時間后,首先觀察到溶液變紅的區域是 (填序號)。
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 | C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某種物質溶于水后得到的溶液中,含有Fe2+、Fe3+、SO42-、NH4+、Ba2+、CO32-離子中的某幾種。
(1)甲同學欲探究溶液的組成,進行了如下實驗:①取少量溶液于試管中,逐滴加入濃氫氧化鈉溶液,發現開始生成白色沉淀,白色沉淀迅速變為灰綠色,最后變為紅褐色,同時伴有刺激性氣體放出;②另取少量溶液于試管中,加入足量鹽酸酸化后再滴加氯化鋇溶液,有白色沉淀生成。
該溶液中一定含有的離子是 ;
寫出①中白色沉淀轉化為紅褐色沉淀的化學方程式 。
(2)乙同學進行如下實驗:取少量溶液于試管中,滴加幾滴硫氰酸鉀溶液,無明顯現象;再滴加H2O2,發現溶液變紅色;繼續滴加H2O2,紅色逐漸褪去且有氣泡產生。為弄清其中緣由,乙同學查閱資料知:
H2O2+SCN-→SO42-+CO2↑+N2↑+H2O+H+
①該反應中,被氧化的元素為 ,每生成lmol CO2轉移的電子數為 NA;
②根據乙同學的實驗現象,請判斷還原性強弱為:Fe2+ SCN-(填<、=或>);
③根據資料,乙同學提出的猜想是:H2O2將SCN-氧化使紅色逐漸褪去。請你設計一個實驗,驗證乙同學的猜想是否正確 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
過氧化物是一類非常重要的化合物,從人們制得第一種過氧化物距今已有200多年的歷史了,在眾多的過氧化物中過氧化氫迄今為止仍然得到廣泛的應用。
(1)與H2O2具有相同的電子總數的雙原子分子有 (寫兩種);
(2)若從海水中提取碘,需將碘化物變成單質碘。寫出在酸性條件下H2O2氧化I—離子的離子方程式 ;
(3)Na2O2、K2O2、CaO2和BaO2都能與酸作用生成H2O2,目前實驗室制取H2O2可通過上述某種過氧化物與適量的稀H2SO4作用并過濾后獲得,其中最適合的過氧化物是 (填化學式);
(4)純H2O2可用作火箭燃料的氧化劑,已知0.4mol液態肼(N2H4)與足量的液態H2O2反應,生成N2(g)和H2O(g),放出256.6kJ的熱量,則該反應的熱化學方程式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某透明澄清溶液可能含有Na+、Fe3+、Ba2+、CO32-、SO32-、SO42-、Cl-、I-等離子中的幾種,為鑒別這些離子,分別取三份少量溶液,按照以下順序進行三個實驗:
實驗①:加CCl4,再滴加少量氯水,振蕩后,CCl4后層變為紫色;
實驗②:加鹽酸后,生成無色無味氣體,該氣體能使飽和石灰水溶液變渾濁;
實驗③:加BaCl2溶液產生白色沉淀,過濾出沉淀,在沉淀中加入足量鹽酸,沉淀不能完全溶解。
(1)分析上述3個實驗,用離子符號寫出每一個實驗得出的結論,可不必完全填滿。
實驗①:含有 ;不含 ;
實驗②:含有 ;不含 ;
實驗③:含有 ;不含 ;
(2)通過上述實驗,不能確定是否存在的離子是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某興趣小組在課外活動中對某溶液進行了多次的檢測,其中的三次檢測結果如下表所示,請回答下列問題:
| | 溶液中檢測出的溶質 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2CO3、NaCl |
| 第三次 | KCl、K2CO3、Na2SO4、NaCl |
| 實驗步驟 | 實驗操作 | 實驗目的 | 反應的離子方程式 |
| 第一步 | 向溶液中滴加過量的硝酸 | 檢驗 ① 的存在 | ② |
| 第二步 | 繼續滴加過量的 ③ 溶液 | 檢驗SO42-的存在 | ④ |
| 第三步 | 過濾,再向濾液中滴加 ⑤ 溶液 | 檢驗 ⑥ 的存在 | Ag++Cl- = AgCl↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
.現有失去標簽的四瓶無色溶液A.B.C.D,只知道它們是K2CO3.K2SO4.H2SO4和Ba(NO3)2,為了鑒別它們,進行如下實驗:
①A+D―→溶液+氣體 ②B+C―→溶液+沉淀
③B+D―→溶液+沉淀 ④A+B―→溶液+沉淀
將④得到的沉淀物加入③所得溶液中,④中沉淀很快溶解并產生無色無味的氣味。
(1)根據以上實驗事實,A.C.D三種無色溶液分別為________、________、________(用化學式表示)。
(2)寫出①②中發生反應的離子方程式:
① ;
② 。
(3)離子反應是中學化學中重要的反應類型,在發生離子反應的反應物或生成物中,一定存在有
①單質 ②氧化物 ③電解質 ④鹽 ⑤化合物
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某電鍍銅廠有兩種廢水需要處理,一種廢水中含有CN-離子,另一種廢水中含有Cr2O72-離子.該廠擬定如圖所示的廢水處理流程。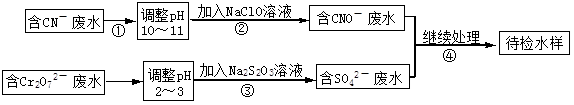 回答以下問題:
回答以下問題:
(1)步驟②發生反應的離子方程式可表示如下:aCN-+bClO-+2cOH-=dCNO-+eN2↑+fCO32-+bCl-+cH2O,上述離子方程式可能的配平系數有多組,請回答:
①方程式中e : f的值為 (填選項標號)。
| A.1 | B.1/2 | C.2 | D.不能確定 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com