
【題目】將7.28g Fe溶于過量的稀H2SO4中,在加熱的條件下,用2.02gKNO3去氧化溶液中Fe2+ , 待反應完全后,剩余Fe2+還需0.4mol/L KMnO4溶液25mL才能完全氧化,則KNO3的還原產物( )
A.NO
B.NO2
C.N2O
D.N2O3
科目:高中化學 來源: 題型:
【題目】三室式電滲析法處理含Na2SO4廢水的原理如圖所示,采用惰性電極,ab、cd均為離子交換膜,在直流電場的作用下,兩膜中間的Na+和SO42﹣可通過離子交換膜,而兩端隔室中離子被阻擋不能進入中間隔室.下列敘述正確的是( ) 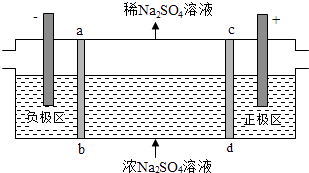
A.通電后中間隔室的SO42﹣離子向正極遷移,正極區溶液pH增大
B.該法在處理含Na2SO4廢水時可以得到NaOH和H2SO4產品
C.負極反應為2H2O﹣4e﹣=O2+4H+ , 負極區溶液pH降低
D.當電路中通過1mol電子的電量時,會有0.5mol的O2生成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含等物質的量NaOH的溶液分別用pH為2和3的CH3COOH溶液中和,設消耗CH3COOH溶液的體積依次為Va、Vb,,則Va、Vb的關系正確的是 ( )
A. Va>10 Vb B. Va=10 Vb C. Vb <10Va D. Vb >10Va
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】臭氧(O3)的制備方法很多,其中電解水法的原理如圖所示,下列有關說法不正確的是( ) 
A.可向水中加入NaCl提高水的導電性
B.b電極周圍pH減小
C.a電極的電極反應式為2H++2e﹣═H2↑
D.a電極為陰極,b電極為陽極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaClO2是一種重要的殺菌消毒劑,也常用來漂白織物等,其一種生產工藝如下: 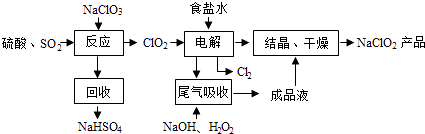
回答下列問題:
(1)NaClO2中Cl的化合價為 .
(2)寫出“反應”步驟中生成ClO2的化學方程式 .
(3)“電解”所用食鹽水由粗鹽水精制而成,精制時,為除去Mg2+和Ca2+ , 要加入的試劑分別為、 . “電解”中陰極反應的主要產物是 .
(4)“尾氣吸收”是吸收“電解”過程排出的少量ClO2 . 此吸收反應中,氧化劑與還原劑的物質的量之比為 , 該反應中氧化產物是 .
(5)“有效氯含量”可用來衡量含氯消毒劑的消毒能力,其定義是:每克含氯消毒劑的氧化能力相當于多少克Cl2的氧化能力.NaClO2的有效氯含量為 . (計算結果保留兩位小數)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于蛋白酶的敘述,不正確的是( )
A. 蛋白酶是蛋白質
B. 蛋白酶的最適pH值是1.9
C. 蛋白酶只能水解蛋白質
D. 蛋白酶在100℃時完全失活
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧、硫、硒、碲都位于元素周期表的VIA族,其化合物在化工生產中有廣泛應用。
(1)下列性質的遞變順序不正確的是_____(填字母)。
A.酸性:H2SeO4>H2SeO3 B.非金屬性:O>S>Se>Te
C.還原性:H2Te>H2Se>H2S>H2O D.熱穩定性:H2O>H2Te>H2Se>H2S
E.沸點: H2Te>H2Se>H2S>H2O
(2)在常溫下進行的置換反應X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的單質,W、V是化合物。
①若W是水,且作還原劑,反應的化學方程式為_________。
②若V是水,為還原產物,反應的化學方程式為_____________。
(3) ①一定溫度下,向恒容密閉容器中充入一定量的H2S,發生反應H2S(g)![]() S2(g)+2H2(g)。下列情況中,可判斷該反應達到平衡狀態的是_______(填字母)。
S2(g)+2H2(g)。下列情況中,可判斷該反應達到平衡狀態的是_______(填字母)。
A.混合氣體的密度不再變化 B.混合氣體的壓強不再變化
C. ![]() 不再變化 D.H2S與H2的消耗速率相等
不再變化 D.H2S與H2的消耗速率相等
②已知:液態CS2完全燃燒生成CO2、SO2氣體,每轉移3mol電子時放出269.2kJ熱量。寫出表示CS2(1)的燃燒熱的熱化學方程式:______________。
(4) ①工業上,用S02還原TeC14溶液制備碲(Te),反應中氧化產物與還原產物的物質的量之比為____________。
②以石墨為電極,電解強堿性Na2TeO3溶液也可獲得碲,電解過程中陰極的電極反應式為_____;陽極產生的氣體是_____ (填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于金屬的說法正確的是( )
A.鋁箔在空氣中受熱可以熔化且會發生劇烈燃燒
B.Na在空氣中燃燒,發出黃色火焰,生成白色固體
C.鐵與水蒸氣反應的產物是黑色的Fe2O3
D.鋁制餐具不能用來盛裝酸、堿、咸的食物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com