
下列各組中,含的離子晶體、分子晶體、原子晶體各一種的是( )
A.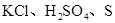 B. 金剛石、
B. 金剛石、
C. HF、SiC、Ar D. 
科目:高中化學 來源: 題型:填空題
氮化鈉(Na3N)是一種實施管制的化學品,它是科學家制備的一種重要的化合物,與水作用可產(chǎn)生NH3。
請回答下列問題:
(1)Na3N的電子式是____________,該化合物是由________鍵形成的。
(2)Na3N與鹽酸反應生成________種鹽,其電子式分別是________。
(3)Na3N與水的反應屬于________(填基本反應類型)反應。
(4)比較Na3N中兩種微粒的半徑:
r(Na+)________r(N3-)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列關于晶體的說法中,不正確的是
①晶體中粒子呈周期性有序排列,有自范性;而非晶體中原子排列相對無序,無自范性;
②含有金屬陽離子的晶體一定是離子晶體;
③共價鍵可決定分子晶體的熔、沸點;
④MgO和NaCl兩種晶體中, MgO的晶格能較小,所以其熔點比較低
⑤晶胞是晶體結構的基本單元,晶體內(nèi)部的微粒按一定規(guī)律作周期性重復排列;
⑥晶體盡可能采取緊密堆積方式,以使其變得比較穩(wěn)定;
⑦干冰晶體中,一個CO2分子周圍有12個CO2分子緊鄰;CsCl和NaCl晶體中陰、陽離子的配位數(shù)不同
| A.①②③ | B.②③⑦ |
| C.④⑤⑥ | D.②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列數(shù)據(jù)是對應物質(zhì)的熔點: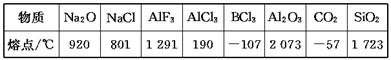
據(jù)此做出的下列判斷中錯誤的是( )
| A.鋁的化合物的晶體中有的是離子晶體 |
| B.表中只有BCl3和干冰是分子晶體 |
| C.同族元素的氧化物可形成不同類型的晶體 |
| D.不同族元素的氧化物可形成相同類型的晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
最近發(fā)現(xiàn)一種鈦原子和碳原子構成的氣態(tài)團簇分子,如圖所示,頂角和面心的原子是鈦原子,棱的中心和體心的原子是碳原子,它的化學式為 ( )
| A.Ti14C13 | B.TiC | C.Ti4C4 | D.Ti4C3 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
據(jù)美國《科學》雜志報道:在40GPa高壓下,用激光器加熱到1800 K,制得具有高熔點、高硬度的二氧化碳晶體。下列關于該晶體的說法正確的是( )
| A.該晶體屬于分子晶體 |
| B.該晶體易汽化,可用作制冷材料 |
| C.一定條件下,該晶體可跟氫氧化鈉反應 |
| D.每摩爾該晶體中含5 mol C—O鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某離子晶體的晶體結構中最小重復單元如圖所示:A為陰離子,在正方體內(nèi),B為陽離子,分別在頂角和面心,則該晶體的化學式為( )。
| A.B2A | B.BA2 | C.B7A4 | D.B4A7 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列對化學知識概括合理的是( )。
| A.原子晶體、離子晶體、金屬晶體、分子晶體中都一定存在化學鍵 |
| B.同素異形體之間的轉(zhuǎn)化都是物理變化 |
| C.原子晶體的熔點不一定比金屬晶體的高,分子晶體的熔點不一定比金屬晶體的低 |
| D.一種元素可能有多種氧化物,但同種化合價只對應一種氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述不正確的是( )
| A.金剛石、碳化硅、晶體硅的熔點依次降低 |
| B.CaO晶體結構與NaCl晶體結構相似,每個CaO晶胞中含有4個Ca2+和4個O2- |
C.設NaCl的摩爾質(zhì)量為M g·mol-1,NaCl的密度為ρ g·cm-3,阿伏加德羅常數(shù)為NA mol-1,在NaCl晶體中,兩個距離最近的Cl-中心間的距離為 · · cm cm |
| D.X、Y可形成立方晶體結構的化合物,其晶胞中X占據(jù)所有棱的中心,Y位于頂角位置,則該晶體的組成式為XY3 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com