
利用海水資源進行化工生產的部分工藝流程如圖: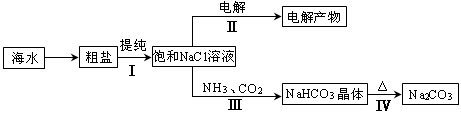
(1)流程I中,欲除去粗鹽中含有的Ca2+、Mg2+、SO42-等離子,需將粗鹽溶解后,按序加入藥品進行沉淀、過濾等。加入藥品和操作的順序可以是 。
a.Na2CO3、NaOH、BaCl2、過濾、鹽酸 b.NaOH、BaCl2、Na2CO3、過濾、鹽酸
c.NaOH、Na2CO3、BaCl2、過濾、鹽酸 d.BaCl2、Na2CO3、NaOH、過濾、鹽酸
(2)流程II中,電解飽和NaCl溶液的離子方程式為 。通電開始后,陽極區產生的氣體是 ,陰極附近溶液pH會 (填“增大”、“減小”或“不變”)。
(3)流程III中,通過反應得到NaHCO3晶體。下圖為NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲線,其中能表示NaHCO3溶解度曲線的是 ,化學反應方程式是 。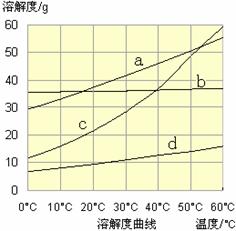
(4)流程IV中,所得純堿常含有少量可溶性雜質,提純它的過程如下:將碳酸鈉樣品加適量水溶解、 、 、過濾、洗滌2-3次,得到純凈Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2=" +473.63" kJ·mol-1
把該過程產生的氣態水完全液化釋放的熱能全部用于生產Na2CO3所需的能耗(不考慮能量損失),若生產1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = 。
(16分)
(1)bd(3分,只選b或d得1分,全對得3分,凡其它有錯答案不得分)。
(2) 2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分,寫“通電”不扣分、漏反應條件、無“↑”、未配平只扣1分); Cl2(或氯氣)(1分),增大(1分)
2OH-+H2↑+Cl2↑(2分,寫“通電”不扣分、漏反應條件、無“↑”、未配平只扣1分); Cl2(或氯氣)(1分),增大(1分)
(3)d (2分) NaCl + CO2 + NH3 + H2O="=" NaHCO3↓+ NH4Cl(2分,未寫“↓”扣1分)
(4)蒸發濃縮 冷卻結晶(2分) — 44.00 kJ/mol(3分,無單位扣1分,沒有符號“-”的不得分)
解析試題分析:(1)a項,雖然能除去雜質及過量碳酸鈉和氫氧化鈉,但是過量氯化鋇沒有除去,故a選項錯誤;b項,既能除去雜質及過量的氫氧化鈉、氯化鋇、碳酸鈉,又不引入新的雜質,故b選項正確;c項,雖然能除去雜質及過量的氫氧化鈉、碳酸鈉,但是過量的氯化鋇沒有除去,故c選項錯誤;d項,既能除去雜質及過量的氯化鋇、碳酸鈉、氫氧化鈉,又不引入新的雜質,故d選項正確;(2)用惰性電解飽和食鹽水可以制備氫氧化鈉、氫氣、氯氣,該反應實質為2Cl-+2H2O 2OH-+H2↑+Cl2↑;陰離子移向陽極,氯離子比氫氧根離子容易失去電子,發生氧化反應,產生黃綠色的氣體,即氯氣;陽離子移向陰極,氫離子比鈉離子容易得到電子,發生還原反應,則陰極產生無色氣體,即氫氣,由于氫離子被消耗,則陰極附近氫離子濃度減小,所以陰極附近溶液的pH增大;(3)流程III的反應屬于復分解反應,即NaCl+NH3+CO2+H2O==NaHCO3↓+NH4Cl(或者NH3+H2O==NH3?H2O、NH3?H2O+CO2==NH4HCO3、NH4HCO3+NaCl="=" NaHCO3↓+NH4Cl),該反應能夠發生的原因是NH4HCO3、NaCl的溶解度均大于NaHCO3,則圖中溶解度最小的d表示NaHCO3;(4)由于被提純物和雜質都是可溶物,雜質可能是NaCl等,根據混合物分離提純的方法推斷,應選擇結晶法分離出碳酸鈉晶體,因此需要將碳酸鈉樣品加適量水溶解、蒸發濃縮、冷卻結晶或降溫結晶、過濾、洗滌,得到純凈的Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉;先將已知兩個熱化學方程式編號為①②,觀察發現①+②可得③Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(g) ΔH3=" +532.36" kJ·mol-1,依題意可知④Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(l) ΔH4=" +92.36" kJ·mol-1,觀察發現(④—③)/10可以得到:H2O(g)="=" H2O(l) ΔH=(ΔH4—ΔH3)/10=" —44" kJ·mol-1。
2OH-+H2↑+Cl2↑;陰離子移向陽極,氯離子比氫氧根離子容易失去電子,發生氧化反應,產生黃綠色的氣體,即氯氣;陽離子移向陰極,氫離子比鈉離子容易得到電子,發生還原反應,則陰極產生無色氣體,即氫氣,由于氫離子被消耗,則陰極附近氫離子濃度減小,所以陰極附近溶液的pH增大;(3)流程III的反應屬于復分解反應,即NaCl+NH3+CO2+H2O==NaHCO3↓+NH4Cl(或者NH3+H2O==NH3?H2O、NH3?H2O+CO2==NH4HCO3、NH4HCO3+NaCl="=" NaHCO3↓+NH4Cl),該反應能夠發生的原因是NH4HCO3、NaCl的溶解度均大于NaHCO3,則圖中溶解度最小的d表示NaHCO3;(4)由于被提純物和雜質都是可溶物,雜質可能是NaCl等,根據混合物分離提純的方法推斷,應選擇結晶法分離出碳酸鈉晶體,因此需要將碳酸鈉樣品加適量水溶解、蒸發濃縮、冷卻結晶或降溫結晶、過濾、洗滌,得到純凈的Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉;先將已知兩個熱化學方程式編號為①②,觀察發現①+②可得③Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(g) ΔH3=" +532.36" kJ·mol-1,依題意可知④Na2CO3·10H2O(s)==Na2CO3 (s)+10H2O(l) ΔH4=" +92.36" kJ·mol-1,觀察發現(④—③)/10可以得到:H2O(g)="=" H2O(l) ΔH=(ΔH4—ΔH3)/10=" —44" kJ·mol-1。
考點:考查物質制備化學工藝流程,涉及粗鹽的分離和提純、電解飽和食鹽水的原理、電極產物及電極附近溶液pH的變化、溶解度曲線在水溶液里復分解反應中的應用、化學方程式、蓋斯定律、熱化學方程式的書寫等。


科目:高中化學 來源: 題型:填空題
工業上合成氨的熱反應方程式如下:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
(1)若已知破壞1mol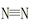 鍵、H—H鍵鍵分別需吸收的能量為946 kJ、436 kJ,則斷開1molN—H需吸收的能量為 kJ。
鍵、H—H鍵鍵分別需吸收的能量為946 kJ、436 kJ,則斷開1molN—H需吸收的能量為 kJ。
(2)在恒溫恒壓的條件下,將2mol N2和6molH2通入一容積可變的容器中反應,達到平衡后氣體的體積為反應前的75%,則該過程釋放的能量為 kJ,氮氣的轉化率為 ,平衡后氨氣占混合氣體的體積分數為 。
(3)若將1mol N2和1molH2通入兩個相同體積的密閉容器甲和乙中,甲容器保持溫度和體積不變,乙容器保持溫度和壓強不變,經過一段時間后,兩容器均達到平衡狀態。
①建立平衡所需的時間:甲 乙(填“>”,“<”或“=”)
②達到平衡后氨氣的體積分數:甲 乙(填“>”,“<”或“=”)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鐵元素是重要的金屬元素,單質鐵在工業和生活中使用得最為廣泛。鐵還有很多重要的化合物及其化學反應。如鐵與水反應:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反應的平衡常數表達式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
則△H=_______。
(3)在t0C時,該反應的平衡常數K=16,在2L恒溫恒容密閉容器甲和乙中,分別按下表所示加入物質,反應經過一段時間后達到平衡。
| | Fe | H2O(g) | Fe3O4 | H2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
| | Fe | H2O(g) | Fe3O4 | H2 |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| | Fe | H2O(g) | Fe3O4 | H2 |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1 | 4 |
| C/mol | m | n | p | q |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氮可以形成多種化合物,如NH3、N2H4、HCN、NH4NO3等。
(1)已知:N2(g)+2H2(g)=N2H4(l) △H=" +" 50.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H="-571.6" kJ·mol-1
則①N2H4(l)+O2(g)=N2(g)+2H2O(l) △H= kJ·mol-1
②N2(g)+2H2(g)=N2H4(l) 不能自發進行的原因是 。
③用次氯酸鈉氧化氨,可以得到N2H4的稀溶液,該反應的化學方程式是 。
(2)采礦廢液中的CN-可用H2O2處理。已知:H2SO4=H++ HSO4- HSO4-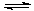 H++ SO42-
H++ SO42-
用鉑電極電解硫酸氫鉀溶液,在陽極上生成S2O82-,S2O82-水解可以得到H2O2。寫出陽極上的電極反應式 。
(3)氧化鎂處理含NH4+的廢水會發生如下反應:
MgO+H2O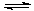 Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+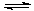 Mg2+ +2NH3·H2O。
Mg2+ +2NH3·H2O。
①溫度對氮處理率的影響如圖所示。在25℃前,升高溫度氮去除率增大的原因是 。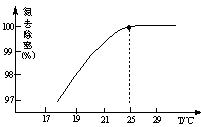
②剩余的氧化鎂,不會對廢水形成二次污染,理由是 。
(4)滴定法測廢水中的氨氮含量(氨氮以游離氨或銨鹽形式存在于水中)步驟如下:①取10 mL廢水水樣于蒸餾燒瓶中,再加蒸餾水至總體積為175 mL②先將水樣調至中性,再加入氧化鎂使水樣呈微堿性,加熱③用25 mL硼酸吸收蒸餾出的氨[2NH3+4H3BO3=(NH4)2B4O7+5H2O]④將吸收液移至錐形瓶中,加入2滴指示劑,用c mol·L-1的硫酸滴定至終點[(NH4)2B4O7+H2SO4+5H2O=(NH4)2SO4+4H3BO3],記錄消耗的體積V mL。則水樣中氮的含量是 mg·L-1(用含c、V的表達式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究硫及其化合物對于工農業生產具有重要意義。
(1)圖Ⅰ所示一個容積為4L的密閉容器,內有可移動的隔板。一定溫度(T)下,左室加入2 mol SO3,右室加入2 mol SO2和1 mol O2,在少量催化劑存在下分別發生反應:
左室:
右室:
反應達到平衡時,右室反應過程和能量關系如圖Ⅱ所示。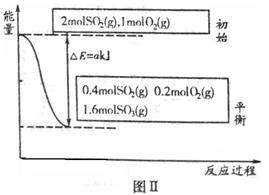
①ΔH2=_______(含a的數學式表示);反應的平衡常數K=_________L·mol-1。
②能說明兩邊反應一定達到平衡的是______________(填序號)。
A.隔板不再移動
B.左右兩邊SO2的物質的量相等
C.左右二室中SO2與O2物質的量之比都是2∶1
③達平衡時,左室反應吸收的熱量為Q1kJ,右室反應吸收的熱量為Q2kJ,則Q1、Q2滿足的關系是_____________(填序號)。
A.Q1=Q2
B.Q1>Q2
C.Q1<Q2
(2)高溫下,熾熱的Cu2S與水蒸氣反應生成金屬銅、H2和SO2(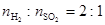 )。
)。
①寫出該反應的化學反應方程式_____________________________________________。
②若有1 mol Cu2S參與反應,則轉移電子的物質的量是_________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
研究NO2.SO2.CO等大氣污染氣體的處理具有重要意義。
(1)NO2可用水吸收,也可用NH3處理,也可用CH4催化還原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用標準狀況下2.24L CH4還原NO2至N2整個過程中轉移的電子總數為______(阿伏加德羅常數的值用NA表示),放出的熱量為______kJ。
(2)已知:2SO2(g)+O2(g) 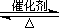 2SO3(g) ?H=-196.6 kJ·mol-1
2SO3(g) ?H=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ?H=-113.0 kJ·mol-1
2NO2(g) ?H=-113.0 kJ·mol-1
(ⅰ)則反應NO2(g)+SO2 (g) SO3(g)+NO(g)的?H= kJ·mol-1。
SO3(g)+NO(g)的?H= kJ·mol-1。
(ⅱ)一定條件下,將NO2與SO2以體積比1:2置于密閉容器中發生上述反應,下列能說明反應達到平衡狀態的是 。
A.每消耗1 mol SO3的同時生成1 mol NO2 B.體系壓強保持不變
C.混合氣體顏色保持不變 D. SO3和NO的體積比保持不變
(ⅲ)某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖(左)所示。
平衡狀態由A變到B時.平衡常數K(A)_______K(B)(填“>”.“<”或“=”)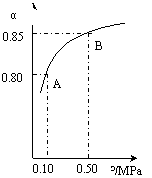
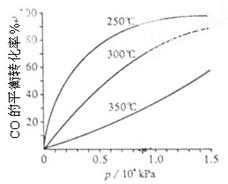
(3)CO可用于合成甲醇,反應方程式為CO(g)+2H2(g) CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。
CH3OH(g)。CO在不同溫度下的平衡轉化率與壓強的關系如上圖(右)所示。該反應?H 0(填“>”或“ <”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
最近幾年我國已加大對氮氧化物排放的控制力度。消除氮氧化物污染有多種方法。
(l)用CH4還原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)與NO2(g)反應生成N2(g)、CO2(g)和H2O(1)的熱化學方程式為 。
(2)用活性炭還原法也可處理氮氧化物。有關反應為:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始時向密閉容器中充入一定量的C(s)和NO2(g),在不同條件下,測得各物質的濃度變化狀況如下圖所示。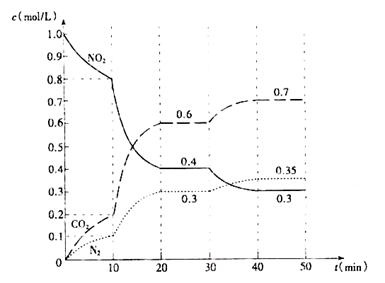
①0?10min內,以CO2表示的平均反應速率v(CO2)= 。
②0~10min,10?20 min,30?40 min三個階段NO2的轉化率分別為α1、α2、α3,其中最小的為 ,其值是 。
③計算反應達到第一次平衡時的平衡常數K= 。
④第10min時,若只改變了影響反應的一個條件,則改變的條件為 (填選項字母)。
A.增加C(s)的量 B.減小容器體積 C.加入催化劑
⑤20~30min、40?50 min時體系的溫度分別為T1和T2,則T1_____T2(填“> “<”或“=”), 判斷的理由是 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(14分)已知用NaAlO2制備α—Al(OH)3及能量轉化關系如圖: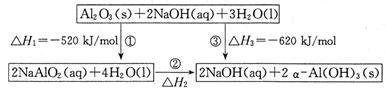
(1)反應②的熱化學方程式為 。
(2)根據上述能量轉化關系,拜耳公司找到了一種簡捷的從鋁土礦獲取Al2O3的方法,流程如下: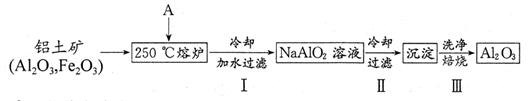
①物質A的化學式為 ;
②步驟Ⅲ的化學反應方程式為 ;檢驗步驟Ⅲ中沉淀是否洗凈的方法是 ;
③步驟Ⅱ采用冷卻的方法析出α—Al(OH)3,該措施的依據是 ;
④工業上可電解上述產物Al2O3以獲得Al,若獲得2.7kgAl,則理論上消耗A的物質的量至少為 mol。有人提出用熔融Na[AlCl4]與NaCl的混合物代替Al2O3進行電解獲得Al,則陰極反應為 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
常溫下鈦的化學活性很小,在較高溫度下可與多種物質反應。
(1)工業上由金紅石(含TiO2大于96%)為原料生產鈦的流程如下: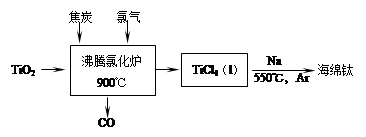
① 沸騰氯化爐中發生的主要反應為: 。
②已知:Ti(s) +2Cl2(g)=TiCl4(l) ΔH=a kJ·mol-1;
2Na(s) +Cl2(g)=2NaCl(s) ΔH=b kJ·mol-1;
Na(s)=Na(l) ΔH=c kJ·mol-1;
則TiCl4(l) +4Na(l)=Ti(s) +4NaCl(s) ΔH= kJ·mol-1。
③ TiCl4遇水強烈水解,寫出其水解的化學方程式 。
(2)TiO2直接電解法生產鈦是一種較先進的方法,電解質為熔融的氯化鈣,原理如圖所示,二氧化鈦電極連接電 極,該極電極反應為: 。但此法會產生有毒氣體,為減少對環境的污染,在電池中加入固體氧離子隔膜(氧離子能順利通過),將兩極產物隔開,再將石墨改為金屬陶瓷電極,并通入一種還原性氣體,該氣體是 。
(3)海綿鈦可用碘提純,原理為: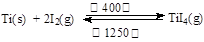 ,下列說法正確的是 。
,下列說法正確的是 。
| A.該反應正反應的ΔH>0 |
| B.在不同溫度區域,TiI4的量保持不變 |
| C.在提純過程中,I2 的作用是將粗鈦從低溫區轉移到高溫區 |
| D.在提純過程中,I2 可循環利用 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com