
������Ч��(y��ng)����ȫ���P(gu��n)ע�ĭh(hu��n)�����}֮һ��CO2��Ŀǰ����к�����ߵ�һ�N���Қ��w����ˣ����ƺ�����CO2�ǽ�Q����Ч��(y��ng)����Ч;����
��1������ͬ����CO(g)��H2O(g)�քeͨ�뵽�w�e��2L�ĺ������]�����У��M(j��n)�з���(y��ng)CO(g)+H2O(g) CO2(g)+H2(g)���õ��������M��(sh��)��(j��)��
CO2(g)+H2(g)���õ��������M��(sh��)��(j��)��
| ��(sh��)�(y��n)�M | �ض�/�� | ��ʼ��/mol | ƽ����/mol | �_(d��)��ƽ������r(sh��)�g/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 ��4����������Դ�ǽ�Q����Ч��(y��ng)��һ�l��Ҫ˼·�����၆�F�LiFePO4��һ�N������܇��x��늳أ�������(y��ng)�飺FePO4+Li LiFePO4��늳��еĹ��w늽��|(zh��)�ɂ���(d��o)Li+���tԓ늳ط�늕r(sh��)�����O��ؓ(f��)�O����(y��ng)ʽ�քe�飺 �� ������ԓ늳�늽����sˮ��늽��늘O�������늘O������(d��ng)늽�ɘO����3360mL���w����(bi��o)��(zh��n)��r���a(ch��n)���r(sh��)��ԓ늳�����䇵��|(zh��)���� ��(Li������(du��)ԭ���|(zh��)���s��7.0)
��4����������Դ�ǽ�Q����Ч��(y��ng)��һ�l��Ҫ˼·�����၆�F�LiFePO4��һ�N������܇��x��늳أ�������(y��ng)�飺FePO4+Li LiFePO4��늳��еĹ��w늽��|(zh��)�ɂ���(d��o)Li+���tԓ늳ط�늕r(sh��)�����O��ؓ(f��)�O����(y��ng)ʽ�քe�飺 �� ������ԓ늳�늽����sˮ��늽��늘O�������늘O������(d��ng)늽�ɘO����3360mL���w����(bi��o)��(zh��n)��r���a(ch��n)���r(sh��)��ԓ늳�����䇵��|(zh��)���� ��(Li������(du��)ԭ���|(zh��)���s��7.0) ��16�֣�
��1����2.67��2�֣� ��<1 ��2�֣� ��< ��2�֣�
��2��5.6��10��5mo1/L ��2�֣�
��3��+172.5 ��2�֣�
��4��FePO4+Li++e��=LiFePO4��2�֣� Li��e��=Li+��2�֣� 1.4 g��2�֣�
����ԇ�}��������1���ٱ��Ќ�(sh��)�(y��n)1���P(gu��n)�M�ֵ���ʼ���|(zh��)������ƽ�����|(zh��)������֪�������w�e��2L������c=n/V���t
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼ��ȣ�mol/L�� 2 1 0 0
׃����ȣ�mol/L�� 0.8 0.8 0.8 0.8
ƽ���ȣ�mol/L�� 1.2 0.2 0.8 0.8
K=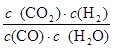 =
=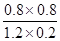 =2.67
=2.67
�ڌ�(sh��)�(y��n)3��CO��H2O����ʼ��ȷքe��a/2mol/L��b/2mol/L���O(sh��)CO��׃����Ȟ�xmol/L������CO��H2O��׃�����֮�ȵ��ڻ��W(xu��)����ʽ��ϵ��(sh��)֮�ȣ��tH2O��׃����Ȟ�xmol/L���tCO��H2O��ƽ���D(zhu��n)���ʷքe��2x/a��2x/b����CO��ƽ���D(zhu��n)���ʴ���ˮ���⣬�t2x/a>2x/b������a/b<1��
���ȸ���(j��)��(sh��)�(y��n)2�����P(gu��n)��(sh��)��(j��)��900�r(sh��)��ƽ�ⳣ��(sh��)���ٸ���(j��)�ضȲ�׃ƽ�ⳣ��(sh��)��׃�����ô˕r(sh��)���M�ֵ����|(zh��)����Ӌ(j��)����ԝ�ȣ�����(j��)������cƽ�ⳣ��(sh��)�Ĵ�С�Д�˕r(sh��)����(y��ng)�M(j��n)�еķ���������̴���ƽ�ⳣ��(sh��)���t����(y��ng)���淴��(y��ng)�����M(j��n)�У���֮���t��������(y��ng)�����M(j��n)�У������(y��ng)���Ă�(g��)�����M(j��n)�У��t�Ă�(g��)��������ʾʹ����෴��������ʡ�
���Ќ�(sh��)�(y��n)2���P(gu��n)�M�ֵ���ʼ���|(zh��)������ƽ�����|(zh��)������֪�������w�e��2L������c=n/V���t
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼ��ȣ�mol/L�� 1 0.5 0 0
׃����ȣ�mol/L�� 0.2 0.2 0.2 0.2
ƽ���ȣ�mol/L�� 0.8 0.3 0.2 0.2
K=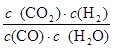 =
=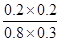 =0.167
=0.167
��(sh��)�(y��n)4�r(sh��)CO��H2O��CO2��H2�ĝ�ȷքe��5mol/L��2.5mol/L��1mol/L��2.5mol/L���tQ=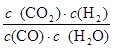 =
=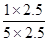 =0.2>K=0.167���f���˕r(sh��)����(y��ng)��(y��ng)ԓ���淴��(y��ng)�����M(j��n)�У�����v(��)>v(��)����v(��)<v(��)��
=0.2>K=0.167���f���˕r(sh��)����(y��ng)��(y��ng)ԓ���淴��(y��ng)�����M(j��n)�У�����v(��)>v(��)����v(��)<v(��)��
��2���O(sh��)���ǰCaCl2��Һ����С��Ȟ�xmol/L��Na2CO3��Һ�ĝ�Ȟ�2��10��4mo1/L���t���w�e��Ϻ�CaCl2��Na2CO3�ĝ�ȷքe��x/2mol/L��1��10��4mo1/L���tKsp=2.8��10��9= x/2��1��10��4��x=5.6��10��5��
��3���Ȍ�3��(g��)�ữ�W(xu��)����ʽ���ξ�̖(h��o)��٢ڢۣ������^���������P(gu��n)ϵ���l(f��)�F(xi��n)��/2����/2=�ۣ��tC(s) + CO2(g) = 2CO(g)�ġ�H3=��H1 /2����H2/2="+172.5" kJ/mol��
��4����늕r(sh��)늳ؿ�����(y��ng)ʽ��FePO4+Li=LiFePO4�������Ԫ����0����+1�r(ji��)���FԪ����+3����+2�r(ji��)��ǰ����ؓ(f��)�O�ϰl(f��)����������(y��ng)�����������O�ϰl(f��)��߀ԭ����(y��ng)������(j��)��ӡ�늺ɡ�ԭ���غ�ԭ����늽��|(zh��)�ж����Ƅ�(d��ng)���x�ӭh(hu��n)�������O����(y��ng)ʽ��FePO4+Li++e��=LiFePO4��ؓ(f��)�O����(y��ng)ʽ��Li��e��=Li+���ö���늘O늽�ˮ��ԭ���2H2O 2H2��+O2����4e�����tn(H2)=2n(O2)������n=V/Vm���tn(H2)+n(O2)="3" n(O2)=3.36L��22.4L/mol=0.15mol���tn(O2)=0.05mol���t�D(zhu��n)����ӵ����|(zh��)����="4" n(O2)=0.2mol����������늳����D(zhu��n)����Ӻ�늽�ˮ�r(sh��)�D(zhu��n)�������ȣ�F(xi��n)ePO4+Li=LiFePO4��e���Ѕ��ӷ���(y��ng)����c�D(zhu��n)����ӵ�ϵ��(sh��)֮�ȵ������|(zh��)����֮�ȣ��t���ӷ���(y��ng)��䇞��0.2mol������䇵�����(du��)ԭ���|(zh��)���s��7.0��m=n��M���t���ӷ���(y��ng)��䇞�1.4g��
2H2��+O2����4e�����tn(H2)=2n(O2)������n=V/Vm���tn(H2)+n(O2)="3" n(O2)=3.36L��22.4L/mol=0.15mol���tn(O2)=0.05mol���t�D(zhu��n)����ӵ����|(zh��)����="4" n(O2)=0.2mol����������늳����D(zhu��n)����Ӻ�늽�ˮ�r(sh��)�D(zhu��n)�������ȣ�F(xi��n)ePO4+Li=LiFePO4��e���Ѕ��ӷ���(y��ng)����c�D(zhu��n)����ӵ�ϵ��(sh��)֮�ȵ������|(zh��)����֮�ȣ��t���ӷ���(y��ng)��䇞��0.2mol������䇵�����(du��)ԭ���|(zh��)���s��7.0��m=n��M���t���ӷ���(y��ng)��䇞�1.4g��
���c(di��n)�����黯�W(xu��)����(y��ng)ԭ�����漰�W(xu��)ƽ�ⳣ��(sh��)�����^����(y��ng)���ƽ���D(zhu��n)���ʡ�������cƽ�ⳣ��(sh��)��С�P(gu��n)ϵ������(y��ng)�M(j��n)�з����c�����淴��(y��ng)���ʴ�С���P(gu��n)ϵ��ϡጶ��ɡ��ܶȷeӋ(j��)�㡢�w˹���ɡ�ԭ늳غ�늽�ԭ����늘O����(y��ng)ʽ�����|(zh��)���������wĦ���w�e��Ħ���|(zh��)�������|(zh��)�����ڻ��W(xu��)���x�ӷ���ʽӋ(j��)���еđ�(y��ng)�õȡ�


 ��x��܇ϵ�д�
��x��܇ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ������}
��15�֣�ij���W(xu��)С�M�����о����l����(du��)���W(xu��)����(y��ng)���ʵ�Ӱ푣��M(j��n)��������(sh��)�(y��n)��
����(sh��)�(y��n)ԭ����2KMnO4 + 5H2C2O4 + 3H2SO4�� K2SO4 + 2MnSO4 + 10CO2�� + 8H2O
����(sh��)�(y��n)��(n��i)�ݼ�ӛ䛡�
| ��(sh��)�(y��n)��̖(h��o) | �Ҝ��£�ԇ��������ԇ���������� / mL | �Ҝ�����Һ�ɫ�����oɫ����r(sh��)�g / min | |||
| 0.6 mol/L H2C2O4��Һ | H2O | 3 mol/L ϡ���� | 0.05mol/L KMnO4��Һ | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |

| ��(sh��)�(y��n)��̖(h��o) | �Ҝ��£�ԇ��������ԇ���������� / mL | ����ԇ���м����������w | �Ҝ�����Һ�ɫ�����oɫ����r(sh��)�g / min | |||
| 0.6 mol/L H2C2O4��Һ | H2O | 3 mol/L ϡ���� | 0.05 mol/L KMnO4��Һ | |||
| 4 | 3.0 | 2.0 | 2.0 | 3.0 | | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
����ʯ�����W(xu��)ʽ��ʾ��MgCO3��CaCO3����ԭ���Ƃ�Mg(OH)2�Ĺ�ˇ�������D��ʾ��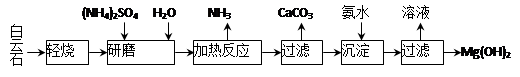
��1����ĥ�������� ��
��2��ԓ��ˇ�п�ѭ�h(hu��n)ʹ�õ����|(zh��)�� �� �������W(xu��)ʽ����
��3������ʯ�p������Ҫ�a(ch��n)����MgO��CaCO3�������y(t��ng)��ˇ�nj�����ʯ�ӟ�ֽ��MgO��CaO����ȡ������ʯ�p���ă�(y��u)�c(di��n)�� ��
��4���ӟᷴ��(y��ng)���x�ӷ���ʽ�� ��
��5���ټӟᷴ��(y��ng)�r(sh��)����323k��353k��Һ��c(NH4+)�c����(y��ng)�r(sh��)�g���P(gu��n)ϵ���D��ʾ��Ո(q��ng)?ji��n)��D����373k��������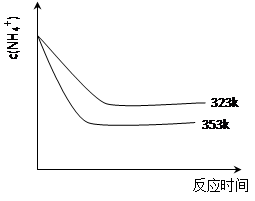
���ɈD��֪���S���ض����ߣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
������܇β���ǜp�ٳ��п՚���Ⱦ�ğ��c(di��n)�о��n�}��
��1����܇��(n��i)ȼ�C(j��)�����r(sh��)�l(f��)���ķ���(y��ng)N2(g) + O2(g) 2NO(g)�����ɵ�NO����܇β�����Ҫ��Ⱦ�T ��r(sh��)����5L���]�����г���6.5 molN2��7.5 molO2����5 min�r(sh��)����(y��ng)�_(d��)��ƽ���B(t��i)���˕r(sh��)������NO�����|(zh��)������5 mol�������]���m(x��)����(y��ng)�����t��
2NO(g)�����ɵ�NO����܇β�����Ҫ��Ⱦ�T ��r(sh��)����5L���]�����г���6.5 molN2��7.5 molO2����5 min�r(sh��)����(y��ng)�_(d��)��ƽ���B(t��i)���˕r(sh��)������NO�����|(zh��)������5 mol�������]���m(x��)����(y��ng)�����t��
��5 min��(n��i)ԓ����(y��ng)��ƽ�����ʦ�(NO) = ����T ��r(sh��)��ԓ����(y��ng)��ƽ�ⳣ��(sh��)K = ��
�� ����(y��ng)�_ʼ���_(d��)��ƽ����^���У����������и��(xi��ng)�l(f��)��׃������ ������̖(h��o)����
a����Ϛ��w���ܶ� b����Ϛ��w�ĉ���(qi��ng)
c��������(y��ng)���� d����λ�r(sh��)�g��(n��i)��N2��NO��������֮��
��2����H2��CO��߀ԭNO�����_(d��)��������Ⱦ��Ŀ�ġ�
��֪��2NO(g) = N2(g) + O2(g) ? ��H =" ��180.5" kJ��mol��1
2H2O(l) =2H2(g) + O2(g) ?��H =" +571.6" kJ��mol��1
�tH2(g)�cNO(g)����(y��ng)����N2(g)��H2O(l)�ğữ�W(xu��)����ʽ��
��
��3����(d��ng)�|(zh��)��һ���r(sh��)��������w�����ı���e������W(xu��)����(y��ng)���ʡ��D��ʾ�������l����׃�r(sh��)������(y��ng)2NO(g) + 2CO(g)
 2CO2(g) + N2(g) �У�NO�ĝ��[c(NO)]�S�ضȣ�T������������e��S���͕r(sh��)�g��t����׃��������
2CO2(g) + N2(g) �У�NO�ĝ��[c(NO)]�S�ضȣ�T������������e��S���͕r(sh��)�g��t����׃��������
�� ԓ����(y��ng)��?H 0 ���������������
���������ı���eS1��S2 �����҈D�Ю���c(NO) ��T1�� S2 �l�����_(d��)��ƽ���^���е�׃����������������(y��ng)��(bi��o)ע����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
�̶�������CO2������Ч�������YԴ�����p�ٿ՚��еĜ��Қ��w�����I(y��)�������о�����CO2�����a(ch��n)�״�ȼ�ϵķ�����ԓ�����Ļ��W(xu��)����ʽ�ǣ�
CO2��g����3H2��g�� CH3OH��g����H2O��g��
CH3OH��g����H2O��g��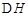 =-49��0kJ��mol
=-49��0kJ��mol
ij�ƌW(xu��)��(sh��)�(y��n)С�M��6mol CO2��8mol H2����һ�ݷe��2L�����]�����У��ضȱ��ֲ�׃�����y(c��)��H2�����|(zh��)�����S�r(sh��)�g׃�����D�Ќ�(sh��)����ʾ���D����ĸ��Ĕ�(sh��)�ֱ�ʾ��(du��)��(y��ng)������(bi��o)�����ش����І��}��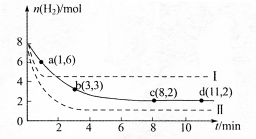
��1��ԓ����(y��ng)��0~8min��(n��i)CO2��ƽ������(y��ng)������ mol��L-1��min-1
��2���˜ض���ԓ����(y��ng)��ƽ�ⳣ��(sh��)K�Ĕ�(sh��)ֵ�� ��
��3���H��׃ijһ�l�����M(j��n)�Ќ�(sh��)�(y��n)���y(c��)��H2�����|(zh��)�����S�r(sh��)�g׃����D��̓����ʾ��
�c��(sh��)����ȣ��������׃�ėl�������� ���������׃�ėl�������� ����(sh��)����(du��)��(y��ng)�l����ƽ�ⳣ��(sh��)��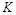 ��������(du��)��(y��ng)�l����ƽ�ⳣ��(sh��)��
��������(du��)��(y��ng)�l����ƽ�ⳣ��(sh��)��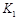 ��������?q��)��?y��ng)�l����ƽ�ⳣ��(sh��)��
��������?q��)��?y��ng)�l����ƽ�ⳣ��(sh��)��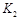 ���t
���t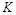 ��
��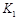 ��
��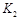 �Ĵ�С�P(gu��n)ϵ�� ��
�Ĵ�С�P(gu��n)ϵ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�Ӌ(j��)���}
2012��2��27���������Q�M(j��n)�롰200�f�v��܇�r(sh��)��������܇β���ѳɞ���Ҫ�Ŀ՚���Ⱦ�
��1����܇��(n��i)ȼ�C(j��)�����r(sh��)����(y��ng)��N2(g)+O2(g) 2NO(g)���nj�(d��o)����܇β���к���NO��ԭ��֮һ��T��r(sh��)����2L���]�����г���4mol N2��6molO2��5min���_(d��)ƽ��r(sh��)NO���|(zh��)������4mol��ԓ����(y��ng)������v(N 2)�� ��Ӌ(j��)��ԓ�l���µ�ƽ�ⳣ��(sh��)������Ӌ(j��)���^�̣���
2NO(g)���nj�(d��o)����܇β���к���NO��ԭ��֮һ��T��r(sh��)����2L���]�����г���4mol N2��6molO2��5min���_(d��)ƽ��r(sh��)NO���|(zh��)������4mol��ԓ����(y��ng)������v(N 2)�� ��Ӌ(j��)��ԓ�l���µ�ƽ�ⳣ��(sh��)������Ӌ(j��)���^�̣���
��2����غ��ݣ����f������(y��ng) 2NO(g)  N2(g)+O2(g) �_(d��)��ƽ����� �����̖(h��o)����
N2(g)+O2(g) �_(d��)��ƽ����� �����̖(h��o)����
| A��NO��N2��O2�ĝ��֮�Ȟ�2��1��1 |
| B��N2�ĝ�Ȳ��ٰl(f��)��׃�� |
| C����λ�r(sh��)�g��(n��i)����2 mol NO��ͬ�r(sh��)����1 mol N2 |
| D��������(n��i)���w�ܶȲ��ٰl(f��)��׃�� |
 2CO2(g)+ N2(g) ��NO�ĝ���S�ض�(T)����������e(S)�͕r(sh��)�g(t)��׃����������(j��)���Д�ԓ����(y��ng)�ġ�H 0 (��������������o���_����)���������ı���eS1��S2 �����D�Ю���NO�ĝ����T1��S2�l�����_(d��)��ƽ���^���е�׃����������ע���l����
2CO2(g)+ N2(g) ��NO�ĝ���S�ض�(T)����������e(S)�͕r(sh��)�g(t)��׃����������(j��)���Д�ԓ����(y��ng)�ġ�H 0 (��������������o���_����)���������ı���eS1��S2 �����D�Ю���NO�ĝ����T1��S2�l�����_(d��)��ƽ���^���е�׃����������ע���l����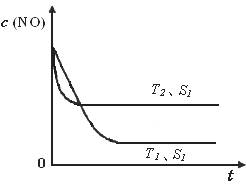
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
��16�֣�Na2S2O8��Һ�ɽ����ЙC(j��)��Ⱦ��4-CP��ԭ����Na2S2O8��Һ��һ���l���¿ɮa(ch��n)����(qi��ng)���������ɻ���SO4-����ͨ�^�y(c��)��4-CP�����ʿ��Д�Na2S2O8��Һ�a(ch��n)����SO4-����������ij�о�С�M̽����Һ��A�ԡ�Fe2+�ĝ�Ȍ�(du��)�a(ch��n)����SO4-������Ӱ푡�
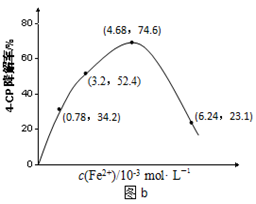
��1����Һ��A�Ե�Ӱ푣������l����ͬ����4-CP���뵽��ͬpH��Na2S2O8��Һ�У��Y(ji��)����Da��ʾ���ɴ˿�֪����Һ��������(qi��ng)�� ���� �������ڡ������ڡ���Na2S2O8�a(ch��n)��SO4-����
��2��Fe2+��ȵ�Ӱ푣���ͬ�l���£�����ͬ��ȵ�FeSO4��Һ�քe����c(4-CP)=1.56��10-4 mol��L��1��c(Na2S2O8)=3.12��10-3 mol��L��1�Ļ����Һ�С�����(y��ng)240 min��y(c��)�Ì�(sh��)�(y��n)�Y(ji��)����Db��ʾ��
��֪ S2O82- + Fe2+= SO4-��+ SO42- + Fe3+������߀���ܕ�(hu��)�l(f��)����SO4-�� + Fe2+��SO42- + Fe3+
�� ��(sh��)�(y��n)�_ʼǰ���z�(y��n)FeSO4��Һ�Ƿ�������ԇ���� �����W(xu��)ʽ�����类���������^�쵽�ĬF(xi��n)���� ��
�ڮ�(d��ng)c(Fe2+)��3.2 ��10-3 mol��L��1�r(sh��)��4-CP�����ʞ� %��4-CP�����ƽ������(y��ng)���ʵ�Ӌ(j��)����_(d��)ʽ�� ��
�ۮ�(d��ng)c(Fe2+)�^��r(sh��)��4-CP�����ʷ����½���ԭ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���(sh��)�(y��n)�}
����^Fe3+��Cu2+��(du��)H2O2�ֽ�Ĵ�Ч����ij���W(xu��)�о�С�M��ͬ�W(xu��)�քe�O(sh��)Ӌ(j��)����D1��2��ʾ�Č�(sh��)�(y��n)��Ո(q��ng)�ش����P(gu��n)���}��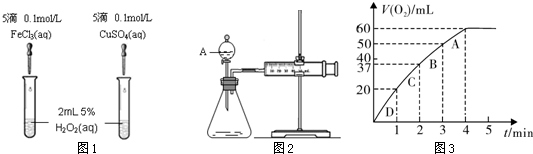
��1�����Է�������D1��ͨ�^�^�� �����Ա��^�ó��Y(ji��)Փ����ͬ�W(xu��)�����FeCl3�Ğ�0.05 mol/L Fe2(SO4)3����������������� ��
��2��������������D2��ʾ����(sh��)�(y��n)�r(sh��)������40 mL���w����������Ӱ푌�(sh��)�(y��n)�����ؾ��Ѻ��ԡ���(sh��)�(y��n)����Ҫ�y(c��)���Ĕ�(sh��)��(j��)�� ��
��3������0.10 mol MnO2��ĩ��50 mL H2O2��Һ�У��ژ�(bi��o)��(zh��n)��r�·ų����w���w�e�͕r(sh��)�g���P(gu��n)ϵ��D3��ʾ��
�ٌ���H2O2�ڶ������i�����°l(f��)������(y��ng)�Ļ��W(xu��)����ʽ ��
�ڌ�(sh��)�(y��n)�r(sh��)�ų����w�Ŀ��w�e�� mL��
��A��B��C��D���c(di��n)����(y��ng)���ʿ��������?y��n)�?u> �� �� �� ��
��ጷ���(y��ng)����׃����ԭ�� ��
��H2O2�ij�ʼ���|(zh��)��������� ��Ո(q��ng)�����λ��Ч��(sh��)�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ����x�}
�����£���amol��L-1�İ�ˮ�cbmol��L-1�}����w�e��ϣ���֪��ͬ�l���°�ˮ����x�̶ȴ���NH4+��ˮ��̶ȣ��t�������P(gu��n)��Փ�����_����
| A������Ϻ���ҺpH=7���tc(NH4+)=c(Cl��) |
| B����b=2a���tc(Cl��)>c(NH4+)>c(H+)>c(OH-) |
| C����a=2b���tc(NH4+)>c(Cl��)>c(OH��)>c(H+) |
| D������Ϻ���Һ�M��c(H+)=c(OH��)+c(NH3��H2O)���t���Ƴ�a=b |
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com