
【題目】救災物資中的一瓶“84消毒液”的包裝說明上有如下信息:含25%NaClO(次氯酸鈉)、1000 mL、密度1.19 g/cm3,稀釋100倍(體積比)后使用。
請回答下列問題:
(1)上述“84消毒液”的物質的量濃度為___mol/L。
(2)該同學取100 mL上述“84消毒液”,稀釋后用于消毒,稀釋100倍后的溶液中c(Na+)=___mol/L(假設稀釋后溶液密度為1.0 g/cm3),該消毒液長時間放置在空氣中能吸收標準狀況下CO2的體積為____L。(已知:酸性:H2CO3> HClO> HCO3-)
(3)災區志愿者根據上述“84消毒液”的包裝說明,欲用NaClO固體(NaClO易吸收空氣中的H2O、CO2)配制480 mL含25%NaClO的消毒液。下列說法正確的是___。
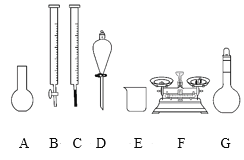
a.如圖所示的儀器中,有四種是不需要的,還需一種玻璃儀器
b.容量瓶用蒸餾水洗凈后,要烘干才能用于溶液的配制
c.利用購買的商品NaClO來配制可能會導致結果偏低
d.需要NaClO固體的質量為143g
(4)ClO2對污水中Fe2+、Mn2+、S2-和CN-等有明顯的去除效果。某工廠污水中含CN-bmg/L,現用ClO2將CN-氧化,只生成兩種無毒氣體,其離子反應方程式為_____,處理100 m3這種污水,至少需要ClO2_____mol。
【答案】4.0 0.04 8.96 C 2ClO2+2CN-===N2+2CO2+2Cl- ![]()
【解析】
(1)根據![]() 可知c(NaClO)=
可知c(NaClO)=![]() =4.0 mol/L。(2)根據稀釋前后溶質的物質的量不變得:100 mL×4.0 mol/L=10 000 mL×c(NaClO),解得稀釋后c(NaClO)=0.04 mol/L,c(Na+)=c(NaClO)=0.04 mol/L。根據NaClO+CO2+H2O=NaHCO3+HClO可知n(CO2)=n(NaClO)=0.4 mol,標準狀況下CO2的體積為8.96 L。(3)A、需用托盤天平稱量NaClO固體,需用燒杯來溶解NaClO,需用玻璃棒進行攪拌和引流,需用容量瓶和膠頭滴管來定容,圖示的A、B、C、D四種儀器不需要,但還需玻璃棒和膠頭滴管等,A錯誤;B、配制過程中需要加入蒸餾水,所以洗滌干凈的容量瓶不必烘干即可使用,B錯誤;C、根據題目信息,由于NaClO易吸收空氣中的H2O、CO2而變質,所以商品NaClO可能部分變質,導致所稱量的固體中NaClO的實際質量可能偏小,從而可能使結果偏低,C正確;D、應選取500 mL容量瓶進行配制,然后取出480 mL即可,所以需要NaClO固體的質量為0.5 L×4.0 mol/L×74.5 g/mol=149.0 g,D錯誤,答案選C。(4)ClO2將CN-氧化為N2和CO2,同時生成Cl-:2ClO2+2CN-=N2+2CO2+2Cl-。100 m3這種污水中含有CN-的質量為100b g,其物質的量為
=4.0 mol/L。(2)根據稀釋前后溶質的物質的量不變得:100 mL×4.0 mol/L=10 000 mL×c(NaClO),解得稀釋后c(NaClO)=0.04 mol/L,c(Na+)=c(NaClO)=0.04 mol/L。根據NaClO+CO2+H2O=NaHCO3+HClO可知n(CO2)=n(NaClO)=0.4 mol,標準狀況下CO2的體積為8.96 L。(3)A、需用托盤天平稱量NaClO固體,需用燒杯來溶解NaClO,需用玻璃棒進行攪拌和引流,需用容量瓶和膠頭滴管來定容,圖示的A、B、C、D四種儀器不需要,但還需玻璃棒和膠頭滴管等,A錯誤;B、配制過程中需要加入蒸餾水,所以洗滌干凈的容量瓶不必烘干即可使用,B錯誤;C、根據題目信息,由于NaClO易吸收空氣中的H2O、CO2而變質,所以商品NaClO可能部分變質,導致所稱量的固體中NaClO的實際質量可能偏小,從而可能使結果偏低,C正確;D、應選取500 mL容量瓶進行配制,然后取出480 mL即可,所以需要NaClO固體的質量為0.5 L×4.0 mol/L×74.5 g/mol=149.0 g,D錯誤,答案選C。(4)ClO2將CN-氧化為N2和CO2,同時生成Cl-:2ClO2+2CN-=N2+2CO2+2Cl-。100 m3這種污水中含有CN-的質量為100b g,其物質的量為![]() ,根據反應方程式可知至少需要消耗ClO2
,根據反應方程式可知至少需要消耗ClO2![]() 。
。


 學練快車道口算心算速算天天練系列答案
學練快車道口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】自從1902年德國化學家哈伯研究出合成氨的方法以來,氮的固定的相關研究獲得了不斷的發展。
(1)下表列舉了不同溫度下大氣固氮的部分平衡常數K值。
反應 | 大氣固氮N2(g)+O2(g) | |
溫度/℃ | 27 | 2260 |
K | 3.84×10-31 | 1 |
①分析數據可知:大氣固氮反應屬于______(填“吸熱”或“放熱”)反應。
②2260℃時,向2 L密閉容器中充入0.3mol N2和0.3mol O2,20 s時反應達平衡。則此 時得到NO____mol,用N2表示的平均反應速率為____。
(2)已知工業固氮反應:N2(g)+3H2(g) ![]() 2NH3 (g) △H<0,在其他條件相同時,分別測定此反應中N2的平衡轉化率隨壓強和溫度(T)變化的曲線如下圖A、B所示,其中 正確的是_____(填“A”或“B”),T1______T2(填“>”或“<”)。
2NH3 (g) △H<0,在其他條件相同時,分別測定此反應中N2的平衡轉化率隨壓強和溫度(T)變化的曲線如下圖A、B所示,其中 正確的是_____(填“A”或“B”),T1______T2(填“>”或“<”)。
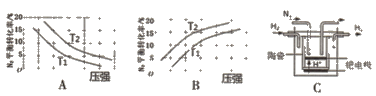
(3)20世紀末,科學家采用高質子導電性的SCY陶瓷(能傳遞H+)為介質,用吸附在它 內外表面上的金屬鈀多晶薄膜做電極,通過電解實現高溫常壓下的電化學合成氨。其示意圖如C所示,陰極的電極反應式為______。
(4)近年,又有科學家提出在常溫、常壓、催化劑等條件下合成氨的新思路,反應原理為:2N2(g)+6H2O(l)![]() 4NH3 (aq) +3O2(g) △H。
4NH3 (aq) +3O2(g) △H。
已知:①N2(g)+3H2(g) ![]() 2NH3(g) △H1
2NH3(g) △H1
②2H2(g) +O2(g) ![]() 2H2O(1) △H2
2H2O(1) △H2
③NH3(g) ![]() NH3(aq) △H3
NH3(aq) △H3
則△H= ________(用含△H1、△H2、△H3的式子表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,物質X2SO4的飽和溶液密度為ρg·mL-1,c(X+)=cmol·L-1 ,溶質 的質量分數為a% ,溶質的摩爾質量為Mg·mol-1,溶解度為Sg,下列表達式正確的是( )
A. c=2000ρa/M B. a%=c/2000ρ
C. M=1000ρa%/c D. S=100cM/(2000ρ-cM)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,體積為2L的密閉容器中,NO2和N2O4之間發生反應,2NO2(g)(紅棕色)![]() N2O4(g)(無色),如圖所示。
N2O4(g)(無色),如圖所示。

(1)曲線____(填“X”或“Y”)表示NO2的物質的量隨時間的變化曲線,
(2)若降低溫度,則v(正)____,v(逆)____.(填“加快"或“減慢"或“不變”)
(3)在0到3min中內X的反應速率為____
(4)達到反應限度時X的轉化率為____,注:物質的轉化率= ![]() ×100%
×100%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用干燥的H2還原WO3制備金屬W的裝置如圖所示(Zn粒中往往含有硫等雜質,焦性沒食子酸溶液用于吸收少量氧氣)。下列說法不正確的是
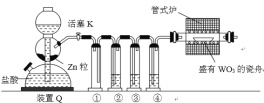
A.①的作用是防倒吸
B.②、③、④中依次盛裝KMnO4溶液、濃H2SO4、焦性沒食子酸溶液
C.管式爐中發生反應的化學方程式為:3H2+ WO3![]() W+3H2O
W+3H2O
D.裝置Q不能用于二氧化錳與濃鹽酸反應制備氯氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z的原子序數依次增加,m、n、p是由這些元素組成的二元化合物,r是一種氣態單質,n為淡黃色粉末,相關物質轉化關系如圖所示。室溫下,0. 0lmol/L的s溶液pH為12,X的質子數是W與Z的質子數之和的一半。下列說法正確的是
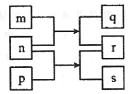
A.原子半徑:W<X<Y
B.簡單氫化物沸點:Z<X<Y
C.n、s中均含有離子鍵和共價鍵
D.q溶于水時溫度升高,證明其水解過程放熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)寫出下列物質的電子式:
NaCl____________;HCl_____________
(2)第三周期元素中的最高價氧化物對應的水化物中,酸性最強的是________,堿性最強的是_____________,呈兩性的氫氧化物是_______________。半徑最大的原子是__________,氫化物最穩定的元素是___________。
(3)硫元素位于元素周期表中______周期_______族,氣態氫化物的化學式是____________,最高價氧化物對應水化物的化學式_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現在正是全球抗擊新冠病毒的關鍵時期,專家指出磷酸氯喹對治療新冠病毒感染有明顯效果,磷酸氯喹的分子結構如圖所示,下列關于該有機物的說法正確的是( )

A.該有機物的分子式為:C18H30N3O8P2Cl
B.該有機物能夠發生加成反應、取代反應、不能發生氧化反應
C.該有機物苯環上的1-溴代物只有2種
D.1mol該有機物最多能和8molNaOH發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.![]() 是“84”消毒液的有效成分,在此次抗擊新冠病毒中發揮了重要作用,請回答下列問題。
是“84”消毒液的有效成分,在此次抗擊新冠病毒中發揮了重要作用,請回答下列問題。
(1)![]() 屬于_____________(填:氧化物,堿,鹽)。
屬于_____________(填:氧化物,堿,鹽)。
(2)浸泡衣物時加入“84”消毒液在空氣中放置一段時間漂白效果更好,原因用離子方程式表示為:______________。(已知酸性:![]() -)
-)
(3)若將“84”消毒液與潔廁靈(主要成分是鹽酸)混合使用,則會產生黃綠色的有毒氣體,其反應的離子方程式是_______。
II.Cl2是一種有毒氣體,如果泄漏會造成嚴重的危害。
(4)已知:![]() ,化工廠可用濃氨水來檢驗Cl2是否泄漏。該反應中被氧化和未被氧化的
,化工廠可用濃氨水來檢驗Cl2是否泄漏。該反應中被氧化和未被氧化的![]() 的物質的量比_______。
的物質的量比_______。
(5)噴射石灰乳等堿性物質可以減輕少量Cl2泄漏造成的危害。Cl2和石灰乳反應的化學方程式是:_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com