
【題目】在接觸法制硫酸的生產中,SO2轉化成SO3轉化率的大小直接決定生產效率。某研究小組用下圖裝置模擬生產過程中測定SO2轉化成SO3的轉化率。已知SO3的熔點是16.8℃,沸點是44.8℃。發生裝置中所涉及反應的化學方程式為:Na2SO3(s)+H2SO4(75%)=Na2SO4+SO2↑+H2O

(1)Ⅱ中的試劑是 ,儀器Ⅵ的名稱為 。
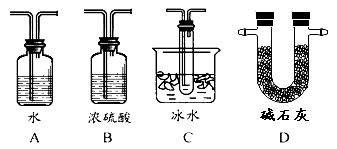
(2)根據實驗需要,應該在Ⅳ、Ⅴ處連接合適的裝置。請從下圖A~D裝置中選擇最適合裝置并將其序號填入下面的空格中,Ⅳ、Ⅴ處連接的裝置分別是 、 。
(3)為了提高SO2的轉化率,實驗時在:①滴加濃硫酸;②加熱催化劑的步驟中,應采取的操作是先_______后_________(填編號)。
(4)實驗結束后,如果把收集SO3的試管敞口露置于空氣中,能夠看到管口有大量的白霧,產生此現象的原因是 。
(5)用12.6gNa2SO3粉末與足量較濃的硫酸進行此實驗,當反應結束時,繼續通入O2一段時間后測得裝置Ⅴ增重了4.48g,則實驗測得SO2的轉化率為 。
【答案】(1)濃硫酸,干燥管(2)C、 D
(3)② ①(4)SO3易揮發,極易溶于水(5)30%
【解析】
試題分析:(1)I中制得的SO2中混有水汽,需要干燥后再進入Ⅲ中,則Ⅱ中盛放濃硫酸干燥SO2氣體,儀器Ⅵ的名稱為干燥管。
(2)SO3的熔點是16,8℃,可以用冰水冷卻來獲得三氧化硫;未反應掉的二氧化硫對空氣會產生污染,可以用堿石灰或者氫氧化鈉溶液來進行尾氣處理,Ⅳ、Ⅴ處連接的裝置分別是C、D;
(3)為了提升SO2的轉化率,實驗時需要先加熱催化劑,再滴加濃硫酸使I中反應開始生成SO2;
(4)SO3易揮發且極易溶解于水,并放出大量熱,則收集SO3的試管敞口露置于空氣中,能夠看到管口有大量的白霧;
(5)根據元素守恒Na2SO3~SO2,則12.6gNa2SO3(即0.1mol)會生成二氧化硫0.1mol,裝置Ⅲ增重了4.48g,說明剩余的二氧化硫為4.48g(即0.07mol),所以二氧化硫的轉化率=(0.1mol-0.7mol)÷0.1mol×100%=30%。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】一定溫度下,在三個容積均為2.0 L的恒容密閉容器中發生反應:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物質的量與反應溫度如下表所示,反應過程中甲、丙容器中CO2的物質的量隨時間變化關系如下圖所示。下列說法正確的是( )
N2(g)+2CO2(g)。各容器中起始物質的量與反應溫度如下表所示,反應過程中甲、丙容器中CO2的物質的量隨時間變化關系如下圖所示。下列說法正確的是( )

容器 | 溫度/℃ | 起始物質的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
A.該反應的正反應為吸熱反應
B.達到平衡時,乙中CO2的體積分數比甲中的小
C.T1℃時,若起始時向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,則反應達到新平衡前v(正)<v(逆)
D.T2℃時,若起始時向丙中充入0.06mol N2和0.12 mol CO2,則達平衡時N2的轉化率大于40%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在10 L密閉容器中進行,半分鐘后,水蒸氣的物質的量增加了0.45 mol,則此反應的平均速率v(X)(反應物的消耗速率或生成物的生成速率)可表示為
4NO(g)+6H2O(g)在10 L密閉容器中進行,半分鐘后,水蒸氣的物質的量增加了0.45 mol,則此反應的平均速率v(X)(反應物的消耗速率或生成物的生成速率)可表示為
A.v(NH3)=0.010 molL-1s-1 B.v(O2)=0.001 molL-1s-1
C.v(NO)=0.0010 molL-1s-1 D.v(H2O)=0.045 molL-1s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.1000 mol/L NaOH溶液分別滴定20.00 mL 0.1000 mol/L鹽酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2條滴定曲線,如下圖所示:
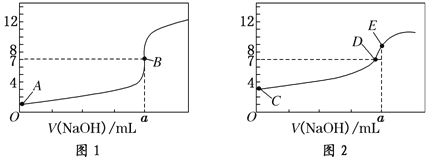
以HA表示酸,下列說法正確的是( )
A.滴定鹽酸的曲線是圖2
B.達到B、D狀態時,兩溶液中離子濃度均為c(Na+)=c(A—)
C.達到B、E狀態時,反應消耗的n( CH3COOH)>n(HCl)
D.當0mL< V(NaOH)<20.00mL時,對應混合溶液中各離子濃度由大到小的順序均為c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器里,A與B反應生成C,其反應速率分別用VA、VB、VC表示,已知2VB=3VA、3 VC =2 VB,則此反應可表示為( )
A. 2A+3B=2C B. A+3B=2C C. 3A+B=2C D. A+B=C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外學習小組對日常生活中不可缺少的調味品M進行探究。已知C可在D中燃燒發出蒼白色火焰。M與其他物質的轉化關系如圖所示(部分產物已略去):
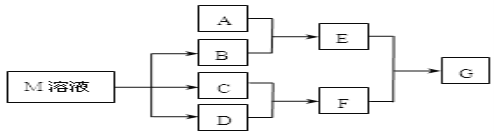
(1)寫出用惰性電極電解M溶液的離子方程式____________。寫出F的電子式____________。
(2)若A是一種常見的酸性氧化物,且可用于制造玻璃,E溶液與F溶液反應可以制備一種膠體,則E溶液的俗稱是___________________。
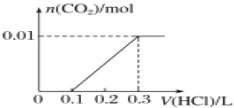
(3)若A是CO2氣體,A與B溶液反應后所得的溶液再與鹽酸反應,放出氣體的物質的量與所加鹽酸體積之間的關系如圖所示,“則A與B溶液”反應后溶液中的溶質為______________(填化學式)。
(4)若A是一種常見金屬單質,且A與B溶液能夠反應,則將過量的F溶液逐滴加入E溶液,邊加邊振蕩,所能觀察到的實驗現象是___________________。
(5)若A是一種不穩定的鹽,A溶液與B溶液混合將產生白色絮狀沉淀且瞬間變為灰綠色,最后變成紅褐色的E,向G溶液中加入苯酚后溶液顯紫色,則由A轉化成E的離子方程式是__________;
(6)若A是一種化肥。實驗室可用A和B反應制取氣體E,E與F、E與D相遇均冒白煙,且利用E與D的反應檢驗輸送D的管道是否泄露,請寫出足量E與D反應的化學方程式________________。
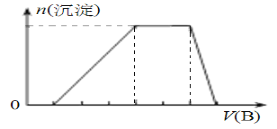
(7)若A是一種溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32﹣中的某些離子,當向該溶液中加入B溶液時發現生成沉淀的物質的量隨B溶液的體積發生變化如圖所示,由此可知,該溶液中肯定含有的離子及其濃度之比為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化氫H2O2,(氧的化合價為-1價),俗名雙氧水,醫療上利用它有殺菌消毒作用來清洗傷口。對于下列A~D涉及H2O2的反應,填寫空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2+H2O
C.2H2O2=2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2僅體現氧化性的反應是(填代號) 。
(2)H2O2既體現氧化性又體現還原性的反應是(填代號) 。
(3)在稀硫酸中,KMnO4和H2O2能發生氧化還原反應。
氧化反應:H2O2-2e-===2H++O2↑
還原反應:MnO![]() +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
寫出該氧化還原反應的化學方程式:_______________________。
(4)請配平以下化學方程式:
![]() Al+
Al+![]() NaNO3+
NaNO3+![]() NaOH===
NaOH===![]() NaAlO2+
NaAlO2+![]() N2↑+
N2↑+![]() H2O
H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨原子序數的遞增,八種短周期元素(用字母表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。
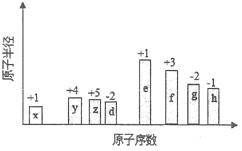
根據判斷出的元素回答問題
(1)g的原子結構示意圖為______________.
(2)比較e、h 簡單離子的半徑大小(用化學式表示,下同),_______>_________ .
比較g 、h 的最高價氧化物對應的水化物的酸性強弱是:_________>____________.
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式__________ .
(4)己知lmole的單質在足量d2中燃燒,恢復至室溫,放出255.5kJ熱量,寫出表示e 的單質燃燒熱的熱化學方程式:__________________________.
(5)上述元素可組成常見的堿性氣體R。回答下列問題:
①.R極易溶于水的原因是(任意寫出兩點):
A.__________________________.
B.__________________________.
② 用方程式表示R 的溶液顯堿性的原因:______________________.
③ 對pH =" 10" 的R 溶液進行下列操作,能使R 的電離平衡逆移的是____________.
A.加入少量 NaCl溶液 B.加入少量1mol.L-1的NH4Cl溶液
C.加入少量MgSO4固體 D.加入少量1mol.L-1 的NaOH溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com