
【題目】下列關于有機物的說法正確的是( )
A.乙醇和丙三醇互為同系物
B.環己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C.分子式為C5H10O2,且屬于酯的同分異構體共有9種(不考慮立體異構)
D.二環己烷( ![]() )的二氯代物有6種結構(不考慮立體異構)
)的二氯代物有6種結構(不考慮立體異構)
【答案】C
【解析】
A.乙醇是飽和一元醇,甘油是飽和三元醇,所含官能團數目不同,因此二者不是同系物,A錯誤;
B.環己烯分子中含有4個飽和碳原子,由于甲烷的分子結構中與該C原子連接的四個原子構成的是四面體結構,所以該物質分子中的所有碳原子不可能同一個平面上,B錯誤;
C.分子式為C5H10O2的酯為飽和一元酯,若為甲酸與丁醇形成的酯有4種,HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;若為乙酸和丙酯,有2種,CH3COOCH2CH2CH3、CH3COOCHCH(CH3)2;若為丙酸和乙醇形成的酯,只有1種,CH3CH2COOCH2CH3;若為丁酸和甲醇形成的酯,有2種,CH3CH2CH2COOCH3、(CH3)2CHCOOCH3,所以屬于酯的同分異構體共有(4+2+1+2)=9種,C正確;
D.二環己烷有2種不同位置的H原子,其二氯取代產物中,若2個Cl原子在同一個C原子上,只有1種結構,若在兩個不同的C原子上,有6種不同的結構,乙醇其二氯代物共有7種,D錯誤;
故合理選項是C。


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:
【題目】氯堿廠電解飽和食鹽水制取NaOH的工藝流程示意圖如下:
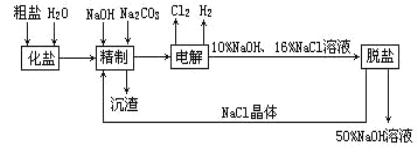
依據上圖,完成下列填空:
(1)在電解過程中,與電源正極相連的電極上所發生的電極反應式為_______;與電源負極相連的電極附近,溶液pH______(選填:不變、升高或下降)。
(2)如果粗鹽中SO42-含量較高,必須加鋇劑除去,該鋇試劑可以是______
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)工業食鹽含Ca2+、Mg2+等雜質,精制過程發生反應的離子方程式為______、_______
(4)電解飽和食鹽水的總反應化學方程式為_________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知短周期元素 A、B、C、D、E 的最高價氧化物對應的水化物分別為 X、Y、M、Z、W,B 是短周期主族元素中原子半徑最大的元素,常溫下 X、Y、Z、W 均可與 M 反應,A、B、D、E 的原子序數及其對應 0.1mol/L X、Y、Z 、W 溶液的 pH 如圖所示。
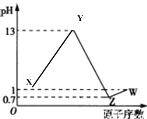
下列說法正確的是:
A. D的簡單氣態氫化物的熱穩定性大于E的氣態氫化物熱穩定性
B. A、B、C 三種元素簡單離子半徑的大小順序為C>B>A
C. Y 的稀溶液與 Z 或 W 的稀溶液分別發生中和反應時,對應的中和熱在數值上相等
D. Y與W 兩物質的化學鍵類型相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】微型銀-鋅電池可用作電子儀器的電源,其電極分別是![]() 和
和![]() ,電解質
,電解質![]() 溶液,電池總反應為
溶液,電池總反應為![]() ,下列說法正確的是( )
,下列說法正確的是( )
A. 電池工作過程中,![]() 溶液濃度降低
溶液濃度降低
B. 電池工作過程中,電解液中![]() 向正極遷移
向正極遷移
C. 負極發生反應![]()
D. 正極發生反應![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米級Cu2O由于具有優良的催化性能而受到關注,下表為制取Cu2O的四種方法:
方法a | 用炭粉在高溫條件下還原CuO |
方法b | 用葡萄糖還原新制的Cu(OH)2制備Cu2O |
方法c | 電解法,反應為 |
方法d | 用肼(N2H4)還原新制的Cu(OH)2 |
(1)已知:①2Cu(s)+![]() O2(g)=Cu2O(s);△H = -169kJ·mol-1
O2(g)=Cu2O(s);△H = -169kJ·mol-1
②C(s)+![]() O2(g)=CO(g);△H = -110.5kJ·mol-1
O2(g)=CO(g);△H = -110.5kJ·mol-1
③Cu(s)+![]() O2(g)=CuO(s);△H = -157kJ·mol-1
O2(g)=CuO(s);△H = -157kJ·mol-1
則方法a發生反應的熱化學方程式是:____________。
(2)方法c采用離子交換膜控制電解液中OH-的濃度而制備納米Cu2O,裝置如圖所示:

該離子交換膜為__________離子交換膜(填“陰”或“陽”),該電池的陽極反應式為___________,鈦極附近的pH值______(填“增大”“減小”或“不變”)。
(3)方法d為加熱條件下用液態肼(N2H4)還原新制Cu(OH)2來制備納米級Cu2O,同時放出N2。該制法的化學方程式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.電解精煉銅時,若轉移2NA個電子,則陽極減少的質量為64g
B.合成氨生產中將NH3液化分離,可加快正反應速率,提高H2的轉化率
C.![]() 在常溫下能自發進行,則該反應的△H>0
在常溫下能自發進行,則該反應的△H>0
D.常溫下,![]() 。欲使溶液中
。欲使溶液中![]() ,需調節溶液的
,需調節溶液的![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是( )
A. 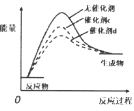 催化劑活性
催化劑活性![]()
B. 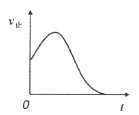
![]()
![]() ,在恒容絕熱容器中投入一定量
,在恒容絕熱容器中投入一定量![]() 和
和![]() ,正反應速率隨時間變化
,正反應速率隨時間變化
C. 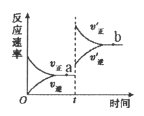
![]()
![]() ,t時刻改變某一條件,則
,t時刻改變某一條件,則![]()
D. 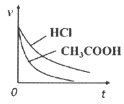 向等體積等pH的HCl和
向等體積等pH的HCl和![]() 中加入等量且足量Zn,反應速率的變化情況
中加入等量且足量Zn,反應速率的變化情況
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用粗鹽(含Ca2+、Mg2+、![]() 等雜質)為主要原料采用“侯氏制堿法”生產純堿和化肥NH4Cl,工藝流程如下圖所示,下列有關說法正確的是( )
等雜質)為主要原料采用“侯氏制堿法”生產純堿和化肥NH4Cl,工藝流程如下圖所示,下列有關說法正確的是( )
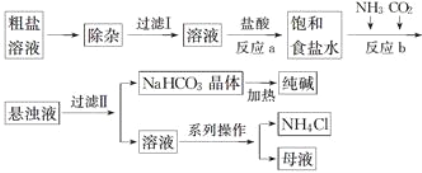
A. 在“侯氏制堿法”中涉及到了氧化還原反應
B. 飽和食鹽水中先通入的氣體為CO2
C. 流程圖中的系列操作中一定需要玻璃棒
D. 工藝中只有碳酸氫鈉加熱分解產生的CO2可回收循環利用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用菱錳礦(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等雜質]為原料制取二氧化錳,其流程示意圖如下:
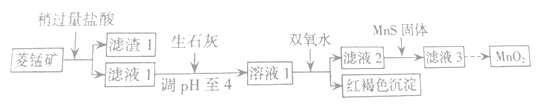
已知生成氫氧化物沉淀的pH:
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
開始沉淀時 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀時 | 9.8 | 8.3 | 3.7 | 6.7 |
注:金屬離子的起始濃度為0.1mol/L
回答下列問題:
(1)含雜質的菱錳礦使用前需將其粉碎,主要目的是_____________;鹽酸溶解MnCO3的離子方程式為___________;
(2)向溶液1中加入雙氧水,反應的離子方程式是 ______________________________;
(3)濾液2中加入稍過量的難溶電解質MnS,以除去Cu2+,反應的離子方程式為_______________;
(4)將MnCl2轉化為MnO2的一種方法是氧化法,其具體做法是用酸化的NaClO3溶液將MnCl2氧化,該反應的離子方程式:5Mn2+ + 2ClO3- + ____ =______+ ____+ ____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com