
【題目】關于膠體的性質與應用,相關說法錯誤的是
A. 靜電除塵器除去空氣或工廠廢氣中的飄塵是利用膠粒的帶電性而加以除去
B. 由于膠粒之間有排斥作用,膠粒不易聚集成大的顆粒,這是膠體具有介穩性的原因之一
C. 泥漿中泥沙是溶質、水是溶劑
D. 膠體的聚沉屬于物理過程
科目:高中化學 來源: 題型:
【題目】H—離子可以跟NH3反應:H— + NH3 = NH2— + H2,根據該反應事實,正確結論是
A. NH3具有還原性 B. H—是很強的氧化劑
C. H2既是氧化產物又是還原產物 D. 該反應屬于置換反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在探究新制飽和氯水成分的實驗中,下列根據實驗現象得出的結論不正確的是
A. 氯水的顏色呈淺黃綠色,說明氯水中含有![]()
B. 干燥氯氣與濕潤氯氣漂白性的對比實驗證明,氯水中具有漂白性的微粒是![]()
C. 向氯水中加入![]() 粉末,有氣泡產生,說明氯水中含有
粉末,有氣泡產生,說明氯水中含有![]()
D. 向![]() 溶液中滴加氯水,溶液顏色變成棕黃色,說明氯水中含有
溶液中滴加氯水,溶液顏色變成棕黃色,說明氯水中含有![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能正確表示下列反應的離子方程式是( )
A. 向次氯酸鈉溶液中通入足量SO2氣體:ClO-+SO2+H2O==HClO+HSO3-
B. 0.1mol/LNH4Al(SO4)2溶液與0.2mol/LBa(OH)2溶液等體積混合: Al3++2SO42-+2Ba2++4OH- =2BaSO4+AlO2-+ 2H2O
C. 用濃鹽酸酸化的KMnO4溶液與H2O2反應,證明H2O2具有還原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
D. Fe2O3溶于過量氫碘酸溶液中:Fe2O3+6H+ +2I-=2Fe2+ +I2 +3H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芳香化合物A、B互為同分異構體,B的結構筒式是 ![]() .A經①、②兩步反應得C、D和E.B經①、②兩步反應得E、F和H.上述反應過程、產物性質及相互關系如圖所示.
.A經①、②兩步反應得C、D和E.B經①、②兩步反應得E、F和H.上述反應過程、產物性質及相互關系如圖所示.
(提示: 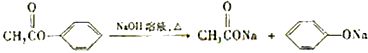 )
)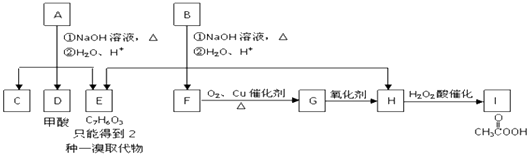
(1)寫出E的結構簡式 .
(2)A有2種可能的結構,寫出相應的結構簡式 .
(3)F和小粒金屬鈉反應的化學方程式是 , 實驗現象是 , 反應類型是 .
(4)寫出F在濃H2SO4作用下在170℃發生反應的化學方程式:實驗現象是 , 反應類型是 .
(5)寫出F與H在加熱和濃H2SO4催化作用下發生反應的化學方程式 , 實驗現象是 , 反應類型是 .
(6)在B、C、D、F、G、I化合物中,互為同系物的是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究化學能與熱能的轉化,某實驗小組設計了如下三套實驗裝置:

(1)上述3個裝置中,不能證明“銅與濃硝酸反應是吸熱反應還是放熱反應”的是___________。
(2)某同學選用裝置Ⅰ進行實驗(實驗前U形管里液面左右相平),在甲試管里加入適量氫氧化鋇溶液與稀硫酸,U形管中可觀察到的現象是_________________,說明該反應屬于_________(填“吸熱”或“放熱”)反應。
(3)為探究固體M溶于水的熱效應,選擇裝置Ⅱ進行實驗(反應在甲中進行)。
①若M為鈉,則實驗過程中燒杯中可觀察到的現象是________________;
②若觀察到燒杯里產生氣泡,則說明M溶于水____________(填“一定是放熱反應”“一定是吸熱反應”或“可能是放熱反應”);
③若觀察到燒杯里的玻璃管內形成一段水柱,則M可能是______。
(4)至少有兩種實驗方法能證明超氧化鉀與水的反應(4KO2+2H2O = 4KOH+3O2↑)是放熱反應還是吸熱反應。
方法(1):選擇上述裝置________(填“Ⅰ”“Ⅱ”或“Ⅲ”)進行實驗;
方法(2):取適量超氧化鉀粉末用脫脂棉包裹并放在石棉網上,向脫脂棉上滴加幾滴蒸餾水,片刻后,若觀察到棉花燃燒,則說明該反應是_____________反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某反應2AB(g)C(g)+3D(g)在高溫時能自發進行,其逆反應在低溫下能自發進行,則該反應的△H、△S應為( )
A.△H<0,△S>0
B.△H<0,△S<0
C.△H>0,△S>0
D.△H>0,△S<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據要求完成下列問題:
(1)某元素原子共有3個價電子,其中一個價電子位于第三能層d軌道,試回答:
該元素核外價電子排布圖 , 該元素基態原子結構示意圖 . 該元素的名稱為 , 形成的單質為晶體.
(2)指出配合物K3[Co(CN)6]中的中心離子、配位體及其配位數:、、 .
(3)試比較下列含氧酸的酸性強弱:H3PO4H3PO3(填“>”、“<”或“=”).
(4)根據價層電子對互斥理論判斷:NH3的電子式為中心原子的雜化方式為
雜化,VSEPR構型為 , 分子的立體構型為 .
(5)在下列物質①CO2、②NH3、③CCl4、④C2H2、⑤H2O、⑥SO2、⑦SO3、⑧、PCl3中,屬于非極性分子的是(填序號).
(6)H2O的沸點(100℃)比H2S的沸點(﹣61℃)高,這是由于 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物M的結構簡式為: 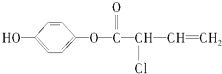 ,有關M的下列敘述中正確的是( )
,有關M的下列敘述中正確的是( )
A.可與H2反應,1 mol M最多消耗5 mol H2
B.可與濃溴水反應,1 mol M最多消耗4 mol Br2
C.可與NaOH溶液反應,1 mol M最多消耗4 mol NaOH
D.M不能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com