
Mg-AgCl電池是一種能被海水激活的一次性貯備電池,電池反應方程式:2AgCl+ Mg = Mg2++ 2Ag +2Cl-。有關該電池的說法正確的是
| A.Mg為電池的正極 |
| B.負極反應為AgCl+e-=Ag+Cl- |
| C.不能被KCl溶液激活 |
| D.可用于海上應急照明供電 |
 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:單選題
有人設計出利用CH4和O2的反應,用鉑電極在KOH溶液中構成原電池。電池的總反應類似于CH4在O2中燃燒,則下列說法正確的是( )
①在標準狀況下,每消耗5.6L CH4可以向外電路提供2mole-
②通過甲烷電極的電極反應式為:CH4+10OH--8e-=CO32-+7H2O
③通過甲烷的電極為電池的正極,通過氧氣的電極為負極
④電池放電后,溶液堿性增強
| A.①② | B.①③ | C.①④ | D.③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
硼化釩(VB2)-空氣電池是目前儲電能力最高的電池,電池示意圖如下,該電池工作時反應為:4VB2 + 11O2→ 4B2O3 + 2V2O5 。下列說法正確的是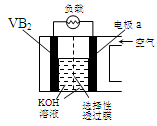
| A.電極a為電池負極 |
| B.圖中選擇性透過膜只能讓陽離子選擇性透過 |
| C.電子由VB2極經KOH溶液流向a電極 |
| D.VB2極發生的電極反應為: |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
銅鋅原電池裝置(見圖),下列分析正確的是
| A.一段時間后兩燒杯中c(Zn2+)、c(Cu2+)均減小 |
| B.原電池工作時,Cu電極流出電子,發生氧化反應 |
| C.原電池工作時的總反應為Zn+Cu2+=Zn2++Cu |
| D.鹽橋中裝有含氯化鉀的瓊脂,其作用是傳遞電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
銀質器皿日久表面會逐漸變黑,這是生成了Ag2S的緣故。根據電化學原理可進行如下處理:在鋁質容器中加入食鹽溶液,再將變黑的銀器浸入該溶液中,一段時間后發現黑色會褪去。下列說法正確的是( )
| A.處理過程中銀器一直保持恒重 |
| B.銀器為正極,Ag2S被還原生成單質銀 |
C.該過程中總反應為2Al+3Ag2S 6Ag+Al2S3 6Ag+Al2S3 |
| D.黑色褪去的原因是黑色Ag2S轉化為白色AgCl |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某原電池的總反應的離子方程式是Zn + Cu2+= Zn2+ + Cu,該原電池的組成正確的是:
| | A | B | C | D |
| 正極 | Zn | Ag | Cu | Cu |
| 負極 | Cu | Cu | Zn | Zn |
| 電解質溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2—CaO作電解質,利用右圖所示裝置獲得金屬鈣,并以鈣為還原劑還原二氧化鈦制備金屬鈦。下列說法中,正確的是 
| A.由TiO2制得1 mol金屬Ti,理論上外電路轉移2 mol電子 |
| B.陽極的電極反應式為C+2O2--4e-=CO2↑ |
| C.在制備金屬鈦前后,整套裝置中CaO的總量減少 |
| D.若用鉛蓄電池作該裝置的供電電源,“+”接線柱應連接Pb電極 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
利用生活中常見的材料可以進行很多科學實驗,甚至制作出一些有實際應用價值的裝置來,如圖就是一個用廢舊材料制作的可用于驅動玩具的電池的示意圖。該電池工作時,有關說法正確的是( )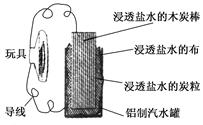
| A.鋁罐將逐漸被腐蝕 |
| B.炭粒和炭棒上發生的反應為O2+4e-=2O2- |
| C.炭棒應與玩具電機的負極相連 |
| D.該電池工作一段時間后炭棒和炭粒的質量會減輕 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com